RESUMEN
Introducción y objetivos: La escala de puntuación PSP (pre-dilation, sizing and post-dilation), derivada del registro GHOST-EU, evalúa la relación entre la técnica de implante de los armazones bioabsorbibles y los resultados clínicos. El objetivo fue realizar una validación externa de la escala PSP y determinar su efecto en eventos adversos cardiacos en diversos escenarios clínicos y anatómicos.
Métodos: Para la validación externa se emplearon los datos del registro REPARA (2.230 pacientes), mientras que se utilizó una base de datos común que combina datos de REPARA y GHOST-EU (3.250 pacientes) para evaluar el efecto de la técnica PSP en varios escenarios clínicos y anatómicos. Se usó PSP-1 y PSP-3 para calificar la calidad de la predilatación, el dimensionamiento de los armazones y la posdilatación. El objetivo primario fue la variable compuesta orientada al dispositivo (muerte cardiaca, infarto de miocardio del vaso diana y revascularización de la lesión diana) a 1 año. También se evaluó la trombosis definitiva o probable del armazón según los criterios del Academic Research Consortium.
Resultados: Se trató a 303 (18,2%) pacientes con una PSP-1 óptima y a 182 (8,2%) con una PSP-3 óptima. La validación externa mostró que la escala PSP tiene un valor predictivo negativo muy alto para el objetivo primario compuesto orientado al dispositivo y la trombosis del armazón (91,8 y 89,1% para PSP-1; 98,4 y 97,3% para PSP-3, respectivamente). En pacientes con PSP-3 óptimo, el objetivo primario compuesto orientado al dispositivo y la trombosis del armazón fueron numéricamente inferiores en comparación con los pacientes sin PSP-3 óptimo (0,5 frente a 2,9%; p = 0,085; y 0,5 frente a 1,8%; p = 0,248, respectivamente). En la base de datos combinada, los beneficios de la escala PSP se observaron en diversos escenarios, excepto en el de infarto de miocardio con elevación del segmento ST, en el que se observó una tendencia hacia laausencia de beneficios de una técnica de PSP óptima (pinteracción = 0,100).
Conclusiones: Una técnica de PSP óptima no se asoció con una tasa más baja del objetivo primario compuesto orientado al dispositivo. Se necesitan nuevos estudios para evaluar el impacto de la técnica de PSP con un seguimiento más prolongado.
Palabras clave: Enfermedad coronaria. Intervención coronaria percutánea. Armazón bioabsorbible. Armazón vascular bioabsorbible.
ABSTRACT
Introduction and objectives: The PSP (pre-dilation, sizing and post-dilation) score, derived from the GHOST-EU registry, has evaluated the relationship between the implantation technique of bioresorbable scaffolds and the clinical outcomes. The objective was to perform an external validation of the PSP technique and to determine its effect on adverse cardiac events in various clinical and anatomical scenarios.
Methods: Data from the REPARA registry (2230 patients) were used for external validation, whereas a common database combining REPARA and GHOST-EU (3250 patients) data was used to evaluate the effect of PSP technique in various clinical and anatomical scenarios. PSP-1 and PSP-3 were used to score the appropriateness of pre-dilation, scaffold sizing, and post-dilation. The primary endpoint was 1-year device-oriented composite endpoint of cardiac death, target-vessel myocardial infarction, and target-lesion revascularization. The definite/probable scaffold thrombosis according to the Academic Research Consortium criteria was also evaluated.
Results: A total of 303 (18.2%) patients were treated with an optimal PSP-1, and 182 (8.2%) with an optimal PSP-3. The external validation showed that PSP has a very high negative predictive value for device-oriented composite endpoint and scaffold thrombosis (91.8% and 89.1% for PSP-1; 98.4% and 97.3% for PSP-3, respectively). Patients with an optimal PSP-3 had a numerically lower rate of device-oriented composite endpoint and scaffold thrombosis compared to those without it (0.5% vs 2.9%; P = .085 and 0.5% vs 1.8%; P = .248, respectively). In the merged database, PSP benefits were seen on many scenarios, except in the ST-segment elevation myocardial infarction where a trend towards no benefit of an optimal PSP technique was present (Pinteraction = .100).
Conclusions: In the REPARA registry, at 1-year follow-up, an optimal PSP technique was not associated with a lower rate of device-oriented composite endpoint. Further research is necessary to assess the impact of the PSP technique in longer follow-ups.
Keywords: Coronary artery disease. Percutaneous coronary intervention. Bioresorbable scaffolds. Bioresorbable vascular scaffolds.
Abbreviations: AVB: armazón vascular bioabsorbible. DOCE: objetivo combinado orientado al dispositivo. PSP: predilatación, dimensionamiento y posdilatación. STEMI: infarto agudo de miocardio con elevación del segmento ST.
INTRODUCCIÓN
Recientes metanálisis de ensayos clínicos aleatorizados han hecho saltar todas las alarmas sobre la seguridad de los armazones vasculares bioabsorbibles (AVB) de primera generación1. En concreto, se halló una tasa de trombosis del armazón más alto de lo esperado comparado con los stents fármacoactivos1-4.
Se propuso optimizar la técnica de implante para mejorar los resultados clínicos de pacientes tratados con AVB5,6. La escala de puntuación PSP (predilatación, dimensionamiento y posdilatación) es un modelo simple diseñado para evaluar la calidad de la técnica de implantación de un AVB, evaluar la preparación de la lesión, el tamaño del armazón y la posdilatación. Este índice se ha desarrollado y validado internamente en el registro GHOST-EU y está asociado a la ocurrencia de eventos cardiovasculares después de un año de seguimiento7. Sin embargo, este índice no ha sido validado externamente ni hay datos disponibles sobre si el efecto de la técnica de implantación PSP varía en diferentes escenarios clínicos y anatómicos.
Nuestro objetivo es realizar la validación externa de la técnica PSP y evaluar su efecto en los eventos adversos cardiacos de pacientes tratados con AVB en diferentes escenarios clínicos y anatómicos.
MÉTODOS
Población
El registro REPARA es un registro multicéntrico, prospectivo, iniciado por investigadores y realizado en 58 centros de España y Portugal. Incluyó pacientes consecutivos sometidos a intervenciones cardiacas percutáneas de uno o varios vasos con, al menos, un dispositivo AVB liberador de everolimus (Absorb BVS; Abbott Vascular, Santa Clara, CA, Estados Unidos). Se consideró como candidatos para la inclusión en el registro a los pacientes sometidos a intervenciones coronarias percutáneas de 1 o 2 (máximo 4) lesiones de arterias coronarias nativas en diferentes vasos epicárdicos. También se incluyó a pacientes que habían sufrido un infarto agudo de miocardio y cuyas lesiones presentaban características específicas complejas. Los datos del registro REPARA se utilizaron para validar externamente la escala de puntuación PSP. Este fue un análisis retrospectivo no preespecificado.
El investigador L. Ortega-Paz recopiló los datos de los registros REPARA y GHOST-EU en una única base de datos para evaluar el efecto de la técnica PSP en diferentes escenarios clínicos y anatómicos. Los detalles del registro GHOST-EU se han descrito con anterioridad7.
Intervenciones y seguimiento
Todas las intervenciones se realizaron de acuerdo con las actuales guías de práctica clínica sobre el abordaje de las intervenciones coronarias percutáneas. En pocas palabras, la predilatación con balón no era obligatoria pero sí estaba altamente recomendada. El implante del armazón a presiones que no excediesen la presión máxima de inflado sí era obligatorio. El uso de la posdilatación se dejó a criterio del operador y en los casos en los que se utilizó, el protocolo recomendaba el uso de un balón no distensible. La angiografía coronaria cuantitativa previa al implante del AVB se analizó en un laboratorio central y solo aquellos pacientes con datos completos de sus angiografías coronarias cuantitativas fueron incluidos en este análisis.
La valoración PSP de la técnica de implantación del AVB se hizo según los modelos mencionados anteriormente7. En líneas generales, se evaluaron tres etapas de implantación de estos armazones en los modelos PSP descritos en la tabla 1. No se hizo una valoración del modelo PSP-2 al no contar con una angiografía coronaria cuantitativa predilatación.
En ambos registros el seguimiento clínico se llevó a cabo mediante visitas médicas o llamadas telefónicas de seguimiento a los 12 meses. En el registro REPARA, el proceso de recogida de datos se monitorizó externamente y los eventos los adjudicó un comité independiente. No se hizo una valoración sistemática de la ocurrencia de infartos de miocardio perioperatorios.
Resultados y definiciones
El objetivo primario fue el combinado orientado al dispositivo (DOCE) de mortalidad cardiaca, infarto de miocardio del vaso diana y revascularización de la lesión diana (RLD) por motivos clínicos. Los objetivos secundarios fueron los componentes individuales del objetivo primario y la trombosis definitiva/probable del stent según los criterios establecidos por la Academic Research Consortium (ARC)8. Los registros REPARA y GHOST-EU usaron las mismas definiciones de los objetivos, siguiendo los criterios de la ARC8. La técnica PSP óptima se definió como el valor más alto obtenido en la escala de puntuación PSP7. En pacientes con más de una lesión tratada, todas las lesiones debían cumplir los criterios de una PSP óptima; de lo contrario, el paciente se clasificaba como no óptimo. Se analizaron todos los objetivos después de un año de seguimiento.
Análisis estadítico
Las variables continuas se expresan como media ± desviación estándar o como mediana y rango intercuartil, según proceda. Las variables categóricas se expresan como número absoluto y porcentaje. Las diferencias detectadas en las proporciones se analizaron con la prueba de la χ2 o la prueba exacta de Fisher y las diferencias de las variables continuas con la prueba t de Student.
La validación externa de la escala de puntuación PSP se llevó a cabo según la validación TRIPOD tipo 49. Las puntuaciones PSP se evaluaron según los términos ya mencionados de rendimiento global, calibración y discriminación10. El rendimiento global de los modelos se valoró utilizando estadísticos de R2 de Nagelkerke10. La calibración se midió con la prueba de Hosmer-Lemeshow10. La discriminación se calculó utilizando el área bajo la curva (AUC) receiver operating characteristic (ROC)10. También se calcularon los valores predictivos y los cocientes de probabilidad10. En la población para validación externa del registro REPARA, el peso de la técnica PSP y de cada componente por separado se calculó utilizando un modelo de regresión de Cox, ajustando para esas variables predictores del DOCE en el análisis univariado: diabetes, infarto de miocardio o revascularización, enfermedad multivaso, lesión gravemente calcificada, bifurcaciones y solapamiento de armazones.
En la base de datos conjunta (datos de los registros REPARA y GHOST-EU), el efecto que tuvo la técnica PSP en el DOCE se evaluó utilizando pruebas de interacción formal en diferentes escenarios clínicos y anatómicos. Estos análisis solo se realizaron con el modelo que dio mejores resultados.
Se utilizó el método Kaplan-Meier para extraer los índices de eventos durante el seguimiento y las curvas de tiempo hasta el evento, dividiendo a la población atendiendo a la técnica PSP óptima o a la puntuación obtenida en cada paso del implante. Se llevó a cabo una comparativa de las curvas de supervivencia de Kaplan-Meier utilizando para ello la prueba de log-rank.
Tabla 1. Modelos PSP para valorar el implante de AVB
| Pasos para el implante | PSP-1 | PSP-2 | PSP-3 |
|---|---|---|---|
| Predilatación | - No realizada - Realizada | - No realizada o realizada con una estenosis residual según la QCA ≥ 30% - Realizada con una estenosis residual según la QCA < 30% | - No realizada - Realizada |
| Dimensionamiento del armazón | Dimensionamiento correcto definido como: - implante de un armazón de 2,5 mm de diámetro en un vaso con un DVR proximal/distal ≥ 2,5 mm y < 2,75 mm - implante de un armazón de 3,0 mm de diámetro en un vaso con un DVR proximal/distal ≥ 2,75 mm and < 3,25 mm o - implante de un armazón de 3,5 mm de diámetro en un vaso con un DVR proximal/distal ≥ 3,25 mm and ≤ 3,75 mm - cuando el DVR proximal y distal eran distintos, se utilizó el valor medio Dimensionamiento incorrecto | ||
| Posdilatación | - No realizada o realizada con un balón distensible o no distensible con un diámetro 0,5 mm mayor que el diámetro del armazón o realizada con un balón NC con un diámetro inferior o igual al diámetro del armazón - Realizada con un balón NC de un diámetro mayor que el del armazón de hasta 0,5 mm | - No realizada o realizada con un balón distensible o no distensible con un diámetro 0,5 mm mayor que el diámetro del armazón o realizada con un balón NC con un diámetro inferior o igual al diámetro del armazón y a una presión < 16 atmósferas - Realizada con un balón NC de un diámetro mayor que el del armazón de hasta 0,5 mm y a una presión ≥ 16 atmósferas | |
AVB: armazon vascular bioabsorbible; DVR: diámetro del vaso de referencia; NC: no distensible; PSP: predilatación, dimensionamiento y posdilatación; QCA: angiografía coronaria cuantitativa. | |||
Los valores de p bilateral (2 colas) < 0,05 se consideraron estadísticamente significativos. Todos los datos se procesaron utilizando el paquete de software estadístico para ciencias sociales, versión 22 (SPSS Inc., Chicago, IL, Estados Unidos).
RESULTADOS
Población para validación externa
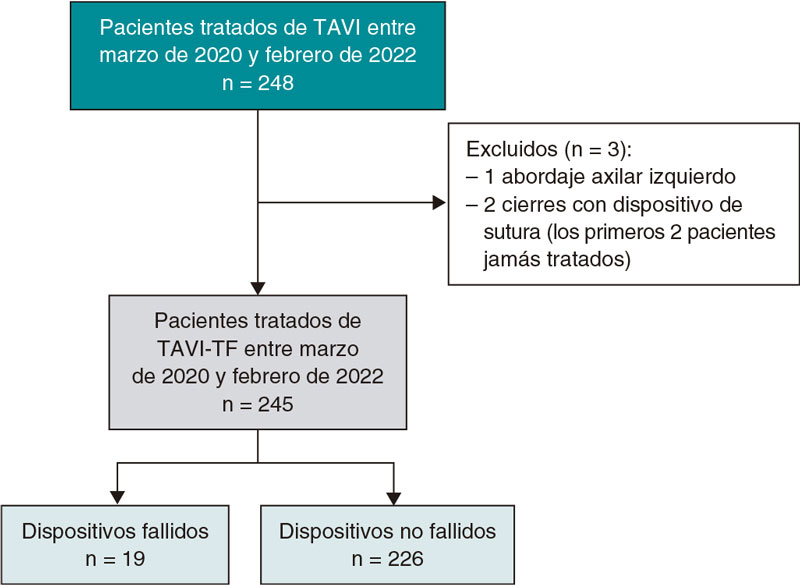
Se incluyó a 2.448 pacientes (3.370 lesiones) en el registro REPARA. Como faltaban datos para poder evaluar los índices PSP-1 y PSP-3, solo se incluyó en este análisis a 2.230 pacientes (2.553 lesiones) (figura 1 del material adicional). No se hizo una valoración de la escala de puntuación PSP-2 porque faltaba el porcentaje de estenosis residual posterior a la predilatación en todos los pacientes, razón por la cual se optó por descartarlo para este análisis. No se observó ninguna diferencia entre los pacientes incluidos y los excluidos en lo que a los resultados clínicos se refiere (datos no mostrados).
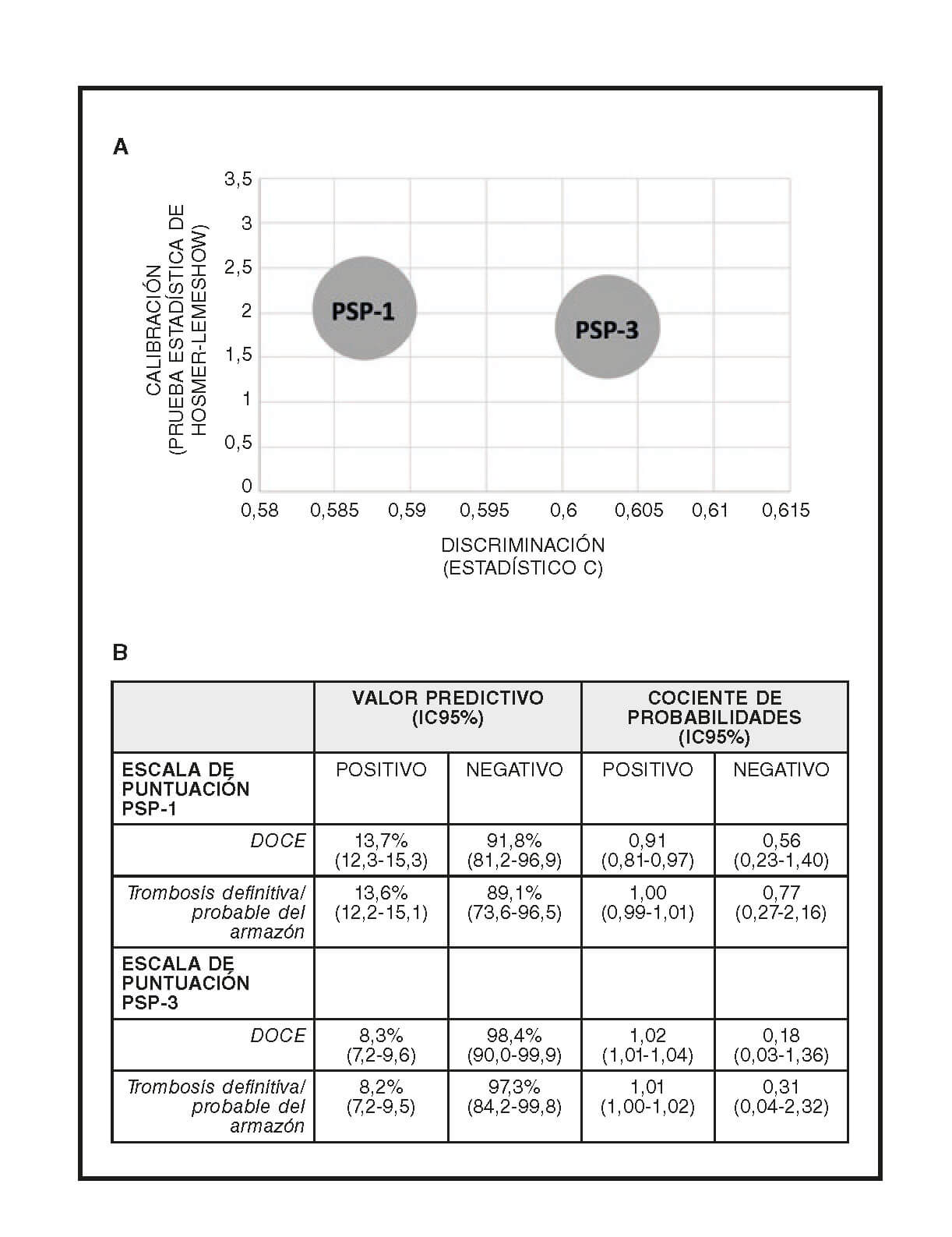
Figura 1. Resultados de los modelos de puntuación PSP. A: Resultados aceptables: PSP- 1: R2: 0,02, HL: X2 = 2,04 (0,727) y AUC: 0,587 (0,511-0,664); p = 0,020. PSP- 3: R2 = 0,03. HL: X2 = 1,84 (0,606) y AUC: 0,603 (0,528-0,677); p = 0,006. B: Resultados descartables. AUC: área bajo la curva receiver operating characteristic (ROC); DOCE: objetivo combinado orientado al dispositivo; HL: Hosmer-Lemeshow (valor p); IC95%: intervalo de confianza del 95%; R2: estadísticos de R2 de Nagelkerke.
Tabla 2. Distribución de los modelos PSP
| PSP-1 (n = 2.553)a | PSP-3 (n = 2.553)a | |
|---|---|---|
| Técnica PSP óptima (%) | 357 (14,0) | 219 (8,6) |
| 1:1 predilatación, n (%) | ||
| No | 497 (19,5) | 497 (19,5) |
| Sí | 2.056 (80,5) | 2.056 (80,5) |
| Dimensionamiento del armazón, n (%) | ||
| Incorrecto | 507 (19,9) | 507 (19,9) |
| 2,50 mm | 135 (26,6) | 135 (26,6) |
| 3,00 mm | 193 (38,1) | 193 (38,1) |
| 3,5 mm | 179 (35,3) | 179 (35,3) |
| Correctob | 2.046 (80,1) | 2.046 (80,1) |
| Posdilatación, n (%) | ||
| No | 1.313 (51,4) | 1.313 (51,4) |
| Sobre-expandidob | 39 (1,5) | 39 (1,5) |
| Balón NC > 1:1b | 623 (24,4) | ND |
| Balón NC > 1:1 a una presión de ≥ 16 atm | ND | 393 (15,4) |
| Análisis QCA preimplante del AVB | ||
| DVR proximal (mm) | 3,10 ± 0,42 | 3,10 ± 0,42 |
| DVR distal (mm) | 2,92 ± 0,55 | 2,92 ± 0,55 |
| DVR medio (mm) | 3,02 ± 0,51 | 3,02 ± 0,51 |
| Longitud de la lesión (mm) | 18,15 ± 9,32 | 18,15 ± 9,32 |
| Estenosis (%) | 84,10 ± 13,1 | 84,10 ± 13,1 |
| DLM (mm) | 0,98 ± 1,15 | 0,98 ± 1,15 |
a Análisis a nivel de la lesión. | ||
Los pacientes tratados con unas técnicas PSP-1 y PSP-3 óptimas fueron 303 (13,6%) y 182 (8,2%), respectivamente (tabla 2; figura 2 del material adicional). Los datos clínicos y procedimentales según la escala de puntuación PSP óptima se describen en la tabla 1 del material adicional, tabla 2 del material adicional, tabla 3 del material adicional y tabla 4 del material adicional.
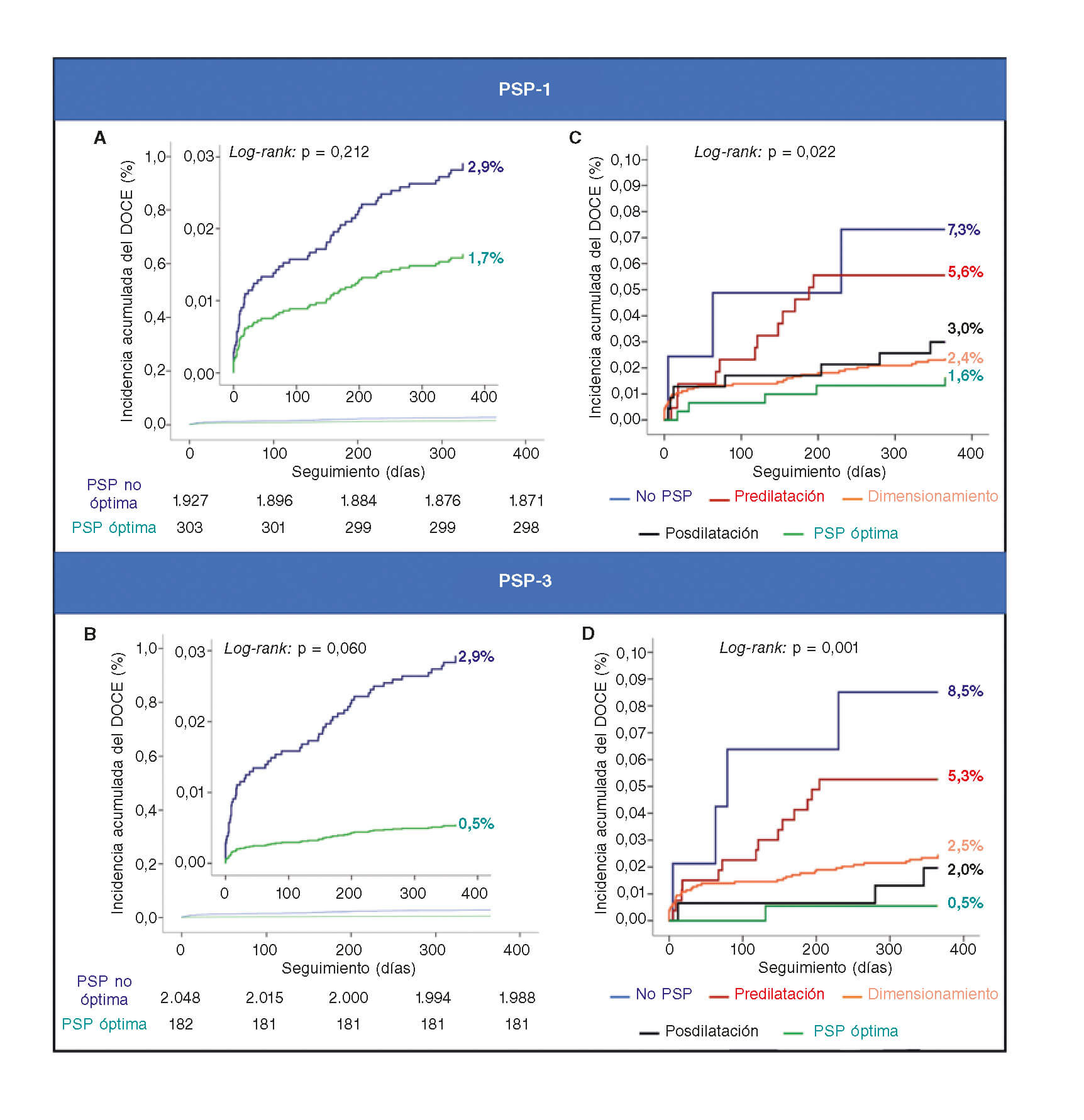
Figura 2. Técnica PSP: análisis Kaplan-Meier. A: PSP-1: eventos agudos (< 24h): el 0% (0/303) frente al 0,3% (6/1.927), log-rank, p = 0,331. Eventos subagudos (1-30 días): el 0,3% (1/303) frente al 0,9% (18/1.921), log-rank, p = 0,286. Eventos tardíos (30-235 días): el 1,3% (4/302) frente al 1,7% (32/1.903), log-rank, p = 0,650. B: predilatación: HR = 1,07; IC95%, 0,58-2,00; p = 0,824. Dimensionamiento del armazón: HR = 0,43; IC95%, 0,25-0,75; p = 0,003. Posdilatación: HR = 0,66; IC95%, 0,34-1,26; p = 0,208. C: PSP-3: eventos agudos (< 24 horas): el 0% (0/182) frente al 0,3% (6/2.048), log-rank, p = 0,465. Eventos subagudos (1-30 días): el 0% (0/182) frente al 0,9% (19/2.042), log-rank, p = 0,192. Eventos tardíos (30-365 días): el 0,5% (1/182) frente al 1,8% (36/2.023), log-rank, p = 0,230. D: predilatación: HR = 1,10; IC95%, 0,59-2,05; p = 0,766. Dimensionamiento del armazón: HR = 0,42; IC95%, 0,24-0,72; p = 0,002. Posdilatación: HR = 0,33; IC95%, 0,12-0,92, p = 0,035. En el análisis a nivel del paciente, el DOCE incluye el IM-VD y la revascularización de la lesión diana. DOCE: objetivo combinado orientado al dispositivo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; IM-VD: infarto de miocardio en el vaso diana; PSP: predilatación, dimensionamien to y posdilatación.
Validación externa
La escala de puntuación PSP-3 fue la que mostró la mejor calibración (X2 = 1,84, p = 0,606 según la prueba estadística de Hosmer-Lemeshow) y discriminación de todas (AUC, 0,603; intervalo de confianza del 95% [IC95%], 0,528–0,677; p = 0,006) (figura 1A). Tanto la escala de puntuación PSP-1 como la PSP-3 arrojaron un valor predictivo negativo alto y un cociente de probabilidades negativo bajo para el DOCE y la trombosis del armazón (figura 1B).
Después de un año de seguimiento, no se observó diferencia alguna en el índice del DOCE entre aquellos pacientes que fueron tratados con una técnica PSP-1 óptima y aquellos que no lo fueron (el 1,6 frente al 2,9%; hazard ratio [HR] = 1,75; IC95%, 0,69–4,45]; p = 0,239, análisis ajustado) (tabla 3). Se observó una tendencia hacia un índice más bajo del DOCE en aquellos pacientes que fueron tratados con una técnica PSP-3 óptima frente a aquellos que no lo fueron (el 0,5 frente al 2,9%; HR = 5,73; IC95%, 0,78–41,88; p = 0,085, análisis ajustado) (tabla 3). La figura 2A y la figura 2B muestran las curvas de supervivencia Kaplan-Meier para el DOCE de las escalas de puntuación PSP.
Dentro de la escala de puntuación PSP-1, el correcto dimensionamiento del armazón se asoció a un descenso del DOCE (HR = 0,43; IC95%, 0,25–0,75; p = 0,003). Dentro de la escala de puntuación PSP-3, el correcto dimensionamiento del armazón (HR = 0,42; IC95%, 0,24–0,72; p = 0,002) o una correcta posdilatación (HR =0,33; IC95%, 0,12–0,92; p = 0,035) se asociaron a un índice más bajo del DOCE (figura 2C, D).
Después de un año de seguimiento, las estrategias simplificadas que solo tuvieron en cuenta la predilatación y la posdilatación según la definición de los modelos PSP-1 (HR = 1,50; IC95%, 0,70–3,19; p = 0,294) y PSP-3 (HR = 1,80; IC95%, 0,65–5,02; p = 0,260) no se asociaron a un índice más bajo del DOCE.
Efecto de una técnica PSP óptima en los diferentes escenarios clínicos y anatómicos
En la base de datos conjunta REPARA y GHOST-EU aquellos pacientes que fueron tratados con la técnica PSP óptima presentaban índices más bajos del DOCE que aquellos que no lo fueron en casi todos los escenarios clínicos y angiográficos analizados. En pacientes con IAMCEST, se observó una tendencia hacia una ausencia de beneficio con la técnica PSP óptima (p para interacción = 0,100) (figura 3).
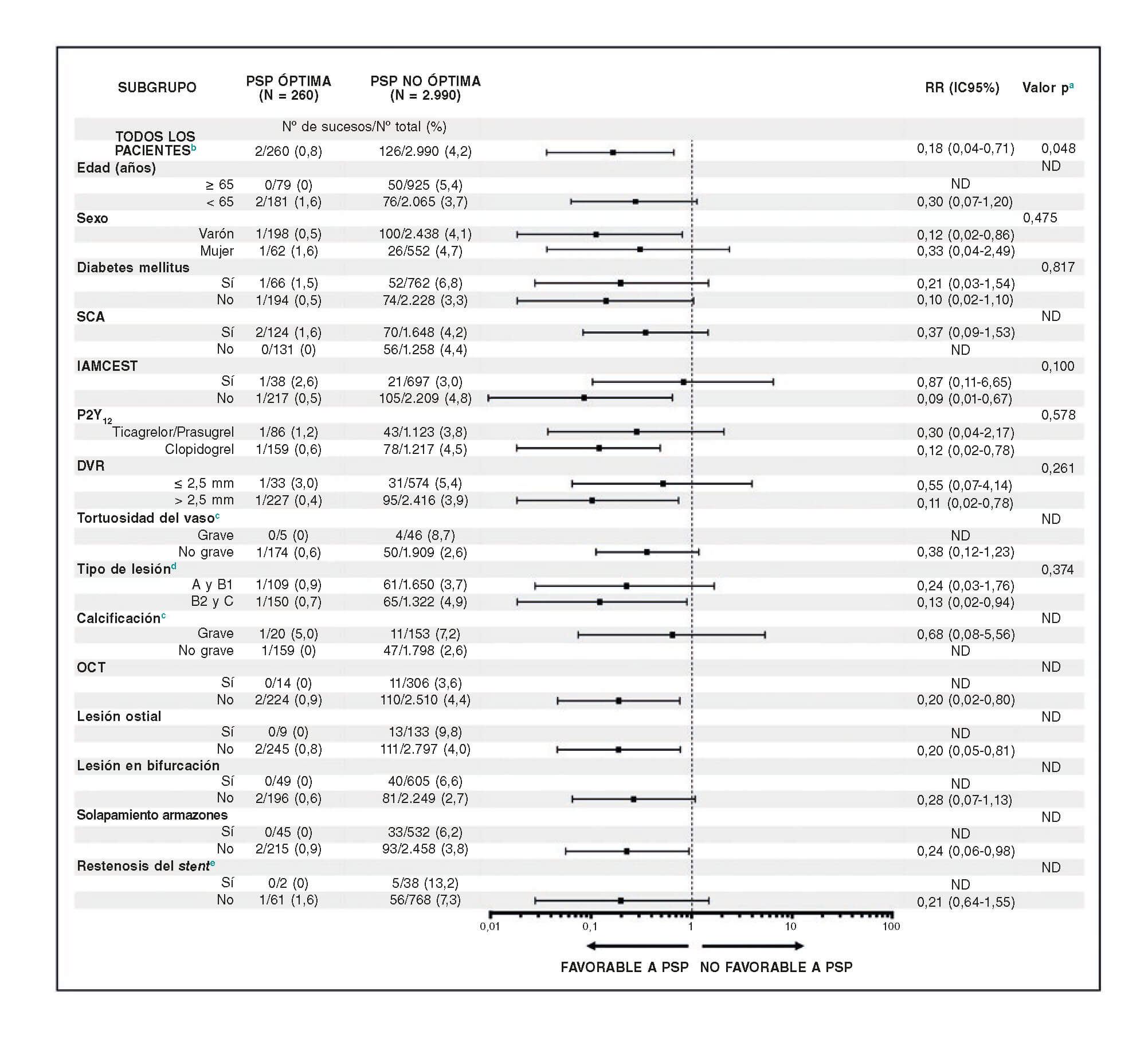
Figura 3. Efecto de una técnica PSP óptima en el DOCE en diferentes escenarios clínicos y anatómicos al año de seguimiento. Análisis conjunto de los registros GHOST-EU y REPARA.
aEl valor p para la interacción representa la probabilidad de interacción entre la variable y una puntuación PSP máxima
bModelo ajustado multivariado.
cDatos solo disponibles del registro REPARA.
dSegún criterios establecidos por el American College of Cardiology-American Heart Association.
eDatos solo disponibles del registro GHOST-EU.
Análisis a nivel del paciente. síndrome coronario agudo
DVR: diámetro del vaso de referencia; IAMCEST: infarto de miocardio con elevación del segmento ST; IC95%: intervalo de confianza del 95%; ND: no disponible; OCT: oclusión coronaria crónica total; PSP: predilatación: dimensionamiento y posdilatación; RR: cociente de tasas de incidencias; SCA: síndrome coronario agudo.
Tabla 3. Resultados clínicos después de un año de seguimiento estratificados según la técnica PSP óptima
| Modelo PSP-1 | ||||
| PSP optima (n = 303)a | PSP no optima (n = 1.927)a | HR (IC95%) | p | |
|---|---|---|---|---|
| DOCEb | 5 (1,7) | 56 (2,9) | 1,75 (0,69-4,45) | 0,219 |
| Mortalidad cardiaca | 1 (0,3) | 14 (0,7) | 2,21 (0,30-16,87) | 0,444 |
| IM-VD | 3 (1,0) | 31 (1,6) | 1,64 (0,50-5,38) | 0,419 |
| RLD | 3 (1,0) | 42 (2,2) | 2,23 (0,69-7,23) | 0,182 |
| Trombosis definitiva/probable del armazón | 4 (1,3) | 33 (1,7) | 1,30 (0,46-3,70) | 0,620 |
| Modelo PSP-3 | ||||
| PSP óptima (n = 182)a | PSP no óptima (n = 2.048)a | HR (IC95%) | p | |
| DOCEb | 1 (0,5) | 60 (2,9) | 5,73 (0,78-41,88) | 0,085 |
| Mortalidad cardiaca | 0 | 15 (0,7) | ND | 0,627 |
| IM-VD | 1 (0,5) | 33 (1,6) | 2,96 (0,40-21,80) | 0,286 |
| RLD | 1 (0,5) | 44 (2,1) | 3,97 (0,54-29,01) | 0,174 |
| Trombosis definitiva/probable del armazón | 1 (0,5) | 36 (1,8) | 3,24 (0,44-23,76) | 0,248 |
aAnálisis a nivel del paciente. | ||||
DISCUSIÓN
Los principales hallazgos de nuestro estudio son: a) una técnica PSP óptima no se asoció a un índice más bajo del DOCE; b) el correcto dimensionamiento del armazón y una correcta posdilatación se asociaron a un índice más bajo del DOCE; c) el efecto que tiene una técnica PSP óptima parece menos importante en el infarto agudo de miocardio con elevación del segmento ST (IAMCEST) que en otros escenarios clínicos y anatómicos (figura 4).
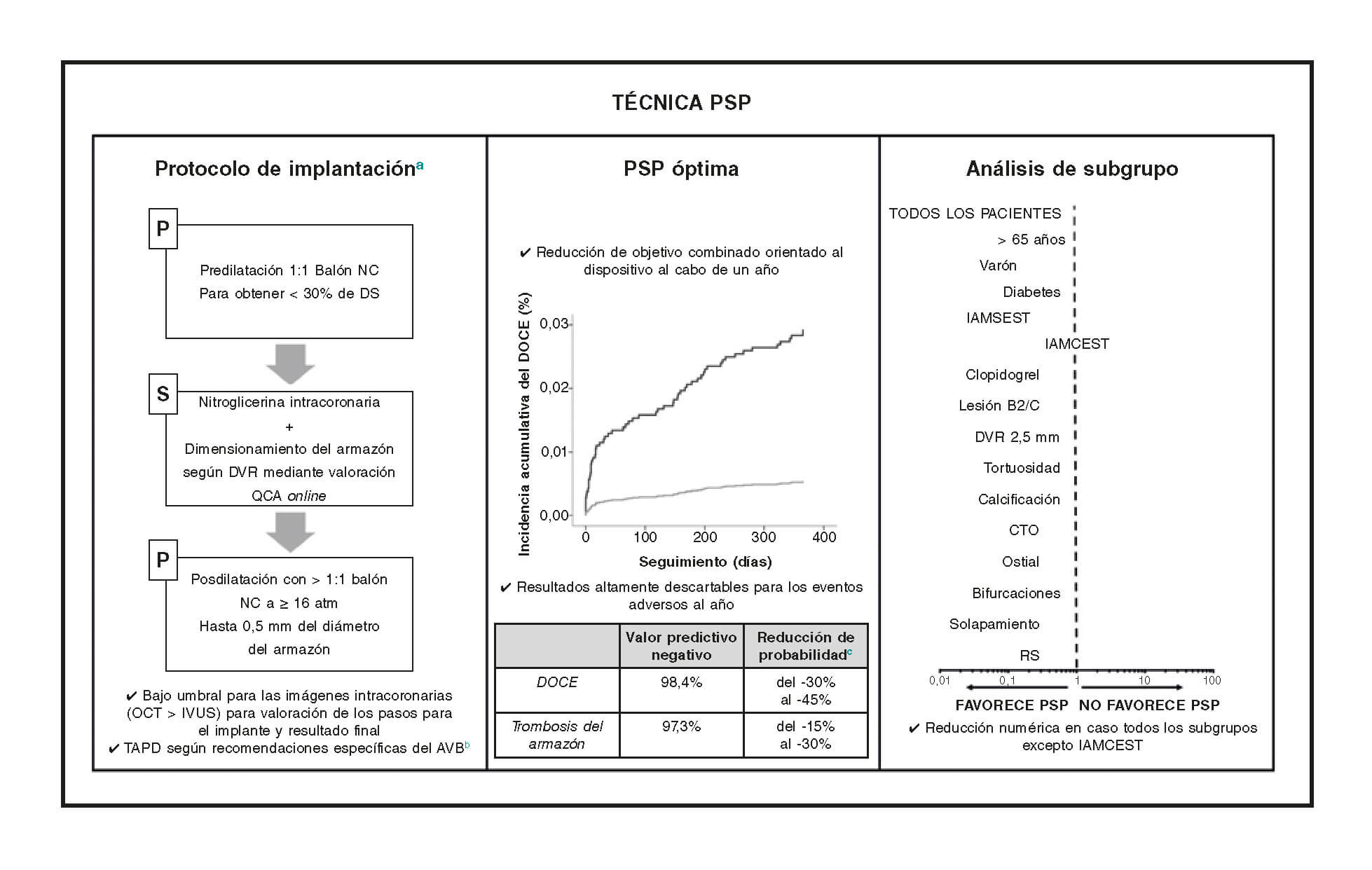
Figura 4. Efecto de la técnica PSP óptima en diferentes escenarios clínicos y anatómicos. En la práctica clínica habitual, la escala de puntuación PSP es un modelo de puntuación simple diseñado para valorar la calidad de la técnica de implantación de un AVB mediante el análisis de tres pasos fundamentales de la técnica PSP. Al cabo de un año de seguimiento, la técnica PSP óptima se asoció a un índice más bajo del DOCE y a un valor predictivo negativo sumamente alto para el DOCE y la trombosis definitiva/probable del armazón. El efecto de la técnica PSP óptima en pacientes IAMCEST parece ser menos importante.
a Se hizo un reporte detallado de las consideraciones operatorias durante el desarrollo y la validación interna7.
b Recomendaciones de expertos sobre TAPD en pacientes tratados con AVB4.
c La reducción de probabilidad se calculó a través de cocientes de probabilidades negativos13.
ATM: atmósferas; AVB: armazón bioabsorbible; CTO: oclusión total crónica; DOCE: objetivo combinado orientado al dispositivo; DS: diámetro de estenosis; DVR: diámetro del vaso de referencia; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IVUS: ecografía intravascular; NC: balón no distensible; OCT: tomografía de coherencia óptica; PSP: predilatación, dimensionamiento y posdilatación; QCA: angiografía coronaria cuantitativa; RS: restenosis del stent; TAPD: tratamiento antiagregante plaquetario doble.
Valor clínico de la técnica PSP en la cohorte de validación
La técnica PSP se ha propuesto para analizar la calidad de la técnica para el implante de AVB con los resultados clínicos7. El presente análisis aplicó la escala de puntuación PSP a la población del registro REPARA en validación externa. Una técnica PSP óptima no se asoció a un índice más bajo del DOCE. Para ser más exactos, una técnica PSP-1 óptima tampoco se asoció a un índice más bajo del DOCE, si bien sí se observó una tendencia hacia un índice más bajo del DOCE en aquellos pacientes que fueron tratados con una técnica PSP-3 óptima. Tanto el índice más bajo del DOCE como la mejora de la técnica podrían guardar relación con este hallazgo. Aunque no pudimos confirmar el efecto que tiene la escala de puntuación PSP sobre los resultados clínicos, creemos que casi toda la literatura médica a este respecto sugiere que una técnica de implantación óptima mejora los resultados. En el análisis de los ensayos ABSORB, el dimensionamiento del vaso y la técnica utilizada por el operador guardaron una estrecha relación con los resultados a los 3 años de seguimiento11. No obstante, otros autores no han encontrado ninguna relación entre la técnica PSP utilizada y los resultados cuando el análisis se realizó a nivel de la lesión12.
Además, en la cohorte de derivación o en esta cohorte de validación, el índice de pacientes tratados con la técnica PSP óptima fue muy bajo (del 13,3 frente al 8,2%, respectivamente)7. Aquí los pacientes tratados con una técnica PSP óptima mostraron una tendencia hacia un índice más bajo de DOCE frente a los que no lo fueron. Aquí deberíamos decir que la técnica PSP arrojó resultados altamente desdeñables con un valor predictivo negativo muy alto y un cociente de probabilidades bajo, lo cual sugiere que un paciente tratado con una técnica PSP óptima tiene una probabilidad de estar libre del DOCE al cabo de un año cercana al 100%10. Los cocientes de probabilidades se utilizan para evaluar la utilidad de realizar una prueba diagnóstica o un modelo de puntuación, asociándose los valores más bajos a una menor probabilidad de un determinado objetivo clínico. Los cocientes de probabilidades negativos sumamente bajos de este análisis significa que una técnica PSP óptima sí se asoció a un descenso entre grande y moderado de ocurrencias del DOCE (del -30 a -45%)13.
Dentro de los pasos individuales de la técnica PSP, el correcto dimensionamiento del armazón se llevó a cabo en un porcentaje más alto de pacientes de esta cohorte de validación que de la cohorte de derivación (un 80% frente a un 50%, respectivamente). Esta mejora podría deberse a la publicación del ensayo ABSORB III entre la publicación de los registros GHOST-EU y REPARA, que arrojó una mayor incidencia de eventos en vasos pequeños14. La importancia del correcto dimensionamiento de los vasos para implantar el AVB se ha detallado, en mayor profundidad, en nuestro análisis, junto a una correcta posdilatación (figura 2).
Efecto de una técnica PSP óptima en diferentes escenarios clínicos y anatómicos
Los datos de que disponemos en la actualidad avalan el uso de la técnica de implantación simplificada para el implante de AVB, pero desconocemos si dicha técnica debería aplicarse a todos los pacientes o a todas las lesiones, o si algún subgrupo de pacientes podría ser el que más se beneficiara de esta técnica5,7. Aunque las lesiones calcificadas precisan, por ejemplo, de una técnica PSP perfecta para optimizar los resultados del AVB, este no es el caso de las lesiones blandas. Por esta razón, en la base de datos conjunta, exploramos el efecto que tiene una técnica PSP óptima en el DOCE en diferentes escenarios clínicos y anatómicos. Resulta interesante que descubriéramos que, en todas las situaciones, los pacientes analizados tratados con una técnica PSP óptima arrojaran un índice más bajo del DOCE que los que no lo fueron. Sin embargo, en pacientes IAMCEST, se observó una tendencia hacia una ausencia de beneficio derivado de una técnica PSP óptima que podría deberse a las particulares características de las lesiones IAMCEST, que suelen ser blandas y trombóticas y precisar una menor preparación de la lesión o posdilatación para reducir la embolización distal15. En pacientes con abundante material trombótico o vasoconstricción coronaria, puede subestimarse el diámetro del vaso; en estas situaciones, acometer la aspiración manual del trombo y el uso de nitroglicerina intracoronaria puede resultar útil y posibilitar el implante de stents más grandes y más cortos16. Un estudio sugiere, por ejemplo, que en pacientes IAMCEST, un leve sobredimensionamiento del armazón da mejores resultados agudos17. También habría que resaltar aquí que el porcentaje de pacientes IAMCEST fue menor en la cohorte de derivación que en la de validación (del 15 frente al 26%, respectivamente): esta diferencia podría haber influido en los resultados de la escala de puntuación en esta determinada situación. Este hallazgo viene avalado por los resultados del estudio BVS STEMI STRATEGY-IT, que analizó una estrategia preespecífica para implantar el armazón vascular bioabsorbible Absorb en pacientes IAMCEST. En este estudio, se observó un índice más bajo del DOCE durante el seguimiento a corto y medio plazo18. Además, un subestudio del STRATEGY-IT, confirmó que una técnica PSP óptima no se asoció a mejores resultados. Cabe destacar aquí que una trombectomía previa al implante óptimo de un AVB revelara una cierta tendencia hacia un mayor diámetro luminal mínimo y una menor huella del armazón19.
Aunque el armazón vascular bioabsorbible Absorb ya no está disponible en la práctica clínica, sí hay en marcha varias evaluaciones clínicas y preclínicas sobre AVB. En los nuevos dispositivos, se desconoce cuál será el efecto de la técnica de implantación, pero si tenemos en cuenta lo similares que son estas tecnologías, parece razonable pensar que la técnica de implantación tendrá, también, un efecto sobre los resultados clínicos.
Limitaciones
Existen algunas limitaciones inherentes a este estudio. En primer lugar, debido al bajo índice de eventos y al uso de la técnica PSP óptima, la relevancia clínica de los valores predictivos podría ser limitada. En segundo lugar, no se dotó a los análisis de subgrupo del potencial estadístico necesario por lo que deberían considerarse, solo, generadores de hipótesis. En tercer lugar, es necesario realizar seguimientos a más largo plazo que validen los modelos de puntuación PSP más allá de seguimientos a un año. A pesar de estas limitaciones, este estudio tiene importantes fortalezas como, por ejemplo, el hecho de ser un extenso registro multicéntrico con muchos criterios de inclusión y pocos criterios de exclusión. En concreto, el registro REPARA posibilitó una completa validación temporal y geográfica de la escala de puntuación, lo que viene a reforzar la metodología de este estudio.
CONCLUSIONES
En el registro REPARA, y después de un año de seguimiento, una técnica PSP óptima no se asoció a un índice más bajo del objetivo combinado orientado al dispositivo. Una técnica PSP óptima arroja un valor predictivo negativo muy alto para el DOCE y la trombosis del armazón. Debemos destacar que, en pacientes IAMCEST, se observó una tendencia hacia una ausencia de beneficio derivada del uso de la técnica PSP óptima. Es necesario realizar estudios de seguimiento más largos que nos analicen el efecto que tiene una técnica PSP óptima tanto en la ocurrencia de eventos muy tardíos como en ámbitos específicos, particularmente el IAMCEST.
FINANCIACIÓN
El registro REPARA está financiado por la Sociedad Española de Cardiología.
CONFLICTO DE INTERESES
R. Moreno y J. Sanchis son Editores Asociados de REC: Interventional Cardiology.
¿QUÉ SE SABE DEL TEMA?
- Se ha propuesto la escala de puntuación PSP para valorar la calidad de la técnica de implantación de armazones bioabsorbibles.
- Optimizar el implante de un AVB puede acarrear menos eventos adversos cardiacos.
¿QUÉ APORTA DE NUEVO?
- En pacientes tratados con la técnica PSP óptima, se observó un descenso del índice de eventos adversos cardiacos. Una puntuación PSP máxima se asoció a un valor predictivo negativo sumamente alto tanto del DOCE como de la trombosis del armazón.
- El efecto de la técnica PSP en pacientes IAMCEST parece menos importante que en otros escenarios clínicos y anatómicos.
- En el futuro, habrá que realizar estudios con seguimientos a más largo plazo para valorar el efecto de la técnica PSP óptima más allá de seguimientos a un año vista.
- El efecto de la técnica PSP óptima sobre los diferentes escenarios clínicos y anatómicos es algo pendiente de confirmación.
- En pacientes IAMCEST, se ha de seguir investigando para desarrollar y validar un protocolo de implantación específico para estos pacientes.
BIBLIOGRAFÍA
1. Ali ZA, Serruys PW, Kimura T, et al. 2-year outcomes with the Absorb bioresorbable scaffold for treatment of coronary artery disease:a systematic review and meta-analysis of seven randomised trials with an individual patient data substudy. Lancet. 2017;390:760-772.
2. Serruys PW, Chevalier B, Sotomi Y, et al. Comparison of an everolimus-eluting bioresorbable scaffold with an everolimus-eluting metallic stent for the treatment of coronary artery stenosis (ABSORB II):a 3 year, randomised, controlled, single-blind, multicentre clinical trial. Lancet. 2016;388:2479-2491.
3. Wykrzykowska JJ, Kraak RP, Hofma SH, et al. Bioresorbable Scaffolds versus Metallic Stents in Routine PCI. N Engl J Med. 2017;376:2319-2328.
4. Capodanno D, Angiolillo DJ. Antiplatelet Therapy After Implantation of Bioresorbable Vascular Scaffolds:A Review of the Published Data, Practical Recommendations, and Future Directions. JACC Cardiovasc Interv. 2017;10:425-437.
5. Puricel S, Cuculi F, Weissner M, et al. Bioresorbable Coronary Scaffold Thrombosis:Multicenter Comprehensive Analysis of Clinical Presentation, Mechanisms, and Predictors. J Am Coll Cardiol. 2016;67:921-931.
6. Tamburino C, Latib A, van Geuns RJ, et al. Contemporary practice and technical aspects in coronary intervention with bioresorbable scaffolds:a European perspective. EuroIntervention. 2015;11:45-52.
7. Ortega-Paz L, Capodanno D, Gori T, et al. Predilation, sizing and post-dilation scoring in patients undergoing everolimus-eluting bioresorbable scaffold implantation for prediction of cardiac adverse events:development and internal validation of the PSP score. EuroIntervention. 2017;12:2110-2117.
8. Cutlip DE, Windecker S, Mehran R, et al. Clinical end points in coronary stent trials:a case for standardized definitions. Circulation. 2007;115:2344-2351.
9. Collins GS, Reitsma JB, Altman DG, and Moons KG. Transparent Reporting of a multivariable prediction model for Individual Prognosis or Diagnosis (TRIPOD):the TRIPOD statement. Ann Inter Med. 2015;162:55-63.
10. Steyerberg EW, Vickers AJ, Cook NR, et al. Assessing the performance of prediction models:a framework for traditional and novel measures. Epidemiology. 2010;21:128-138.
11. Stone GW, Abizaid A, Onuma Y, et al. Effect of Technique on Outcomes Following Bioresorbable Vascular Scaffold Implantation:Analysis From the ABSORB Trials. J Am Coll Cardiol. 2017;70:2863-2874.
12. Tijssen RYG, Kraak RP, Elias J, et al. Implantation techniques (predilatation, sizing, and post-dilatation) and the incidence of scaffold thrombosis and revascularisation in lesions treated with an everolimus-eluting bioresorbable vascular scaffold:insights from the AIDA trial. EuroIntervention. 2018;14:e434-e442.
13. McGee S. Simplifying likelihood ratios. J Gen Intern Med. 2002;17:646-649.
14. Steinvil A, Rogers T, Torguson R, and Waksman R. Overview of the 2016 U.S. Food and Drug Administration Circulatory System Devices Advisory Panel Meeting on the Absorb Bioresorbable Vascular Scaffold System. JACC Cardiovasc Interv. 2016;9:1757-1764.
15. Zhang ZJ, Marroquin OC, Stone RA, et al. Differential effects of post-dilation after stent deployment in patients presenting with and without acute myocardial infarction. Am Heart J. 2010;160:979-986 e1.
16. Fernandez-Rodriguez D, Regueiro A, Brugaletta S, et al. Optimization in stent implantation by manual thrombus aspiration in ST-segment-elevation myocardial infarction:findings from the EXAMINATION trial. Circ Cardiovasc Interv. 2014;7:294-300.
17. Kocka V, Maly M, Tousek P, et al. Bioresorbable vascular scaffolds in acute ST-segment elevation myocardial infarction:a prospective multicentre study 'Prague 19'. Eur Heart J. 2014;35:787-794.
18. Ielasi A, Campo G, Rapetto C, et al. A Prospective Evaluation of a Pre-Specified Absorb BVS Implantation Strategy in ST-Segment Elevation Myocardial Infarction:The BVS STEMI STRATEGY-IT Study. JACC Cardiovasc. Interv. 2017;10:1855-1864.
19. Hioki H, Brugaletta S, Ishida K, et al. Impact of Absorb bioresorbable scaffold implantation technique on post-procedural quantitative coronary angiographic endpoints in ST-elevation myocardial infarction:a sub-analysis of the BVS STEMI STRATEGY-IT study. EuroIntervention. 2018. http://dx.doi.org/10.4244/EIJ-D-18-00504.
Autor para correspondencia: Servei de Cardiologia, Hospital Clinic, Institut d’Investigacions Biomèdiques August Pi i Sunyer (IDIBAPS), Villarroel 170, 08036 Barcelona, España.
Correo electrónico: sabrugal@clinic.ub.es (S. Brugaletta).