Durante la segunda mitad de 2019 se inició en nuestro país la comercialización del cangrelor, un «nuevo» antiagregante plaquetario con características farmacológicas singulares que lo hacen atractivo para determinadas situaciones clínicas en el contexto de la intervención coronaria percutánea (ICP). Cabe entrecomillar lo de «nuevo» porque el ensayo clínico que demostró su superioridad frente al clopidogrel en la ICP, el CHAMPION PHOENIX1, se publicó en 2013 y su aprobación por los organismos reguladores se produjo en 2015. Esta demora ha hecho que la evidencia científica sobre el fármaco no esté de rabiosa actualidad y, por ende, que no esté bien interiorizada en toda la comunidad cardiológica en el momento actual. Además, la indicación especificada en la ficha técnica está basada exclusivamente en las condiciones del ensayo clínico que motivó su aprobación (como es, por otro lado, preceptivo) y no en las de la práctica en la vida real, lo que puede generar ciertas dudas en el momento de seleccionar los pacientes que podrían beneficiarse del fármaco2.
En resumen, el cangrelor es un antagonista intravenoso del receptor plaquetario P2Y12 del difosfato de adenosina, al que se une de forma directa (sin necesidad de conversión en un metabolito activo), reversible y con gran afinidad. En términos farmacodinámicos, las propiedades del cangrelor son: a) inicio de acción muy rápido (3-6 minutos); b) efecto dependiente de la dosis y muy potente (inhibición > 90% de la vía del receptor P2Y12) a la dosis empleada en la ICP; y c) cese rápido de la acción (vida media corta, de 3-5 minutos), con recuperación de la función plaquetaria basal en 60-90 minutos tras finalizar la infusión3.
Dadas sus características farmacológicas, el cangrelor podría contribuir a solventar ciertos problemas que presentan otros agentes antiagregantes. Por ejemplo, los inhibidores del receptor P2Y12 (iP2Y12) orales, en especial el clopidogrel y en menor medida el prasugrel y el ticagrelor, presentan una demora en alcanzar una inhibición plaquetaria óptima, que es más acusada en determinados escenarios como el del infarto de miocardio con elevación del segmento ST (IAMCEST), en el que la biodisponibilidad de los fármacos orales puede estar comprometida (peor absorción intestinal, vómitos, uso de opiáceos o situaciones como intubación, hipotermia terapéutica o shock cardiogénico)3,4. Además, el uso de fármacos parenterales inhibidores de la glucoproteína IIb/IIIa, a pesar de su eficacia para reducir eventos trombóticos, puede asociarse con un aumento del riesgo hemorrágico.
El desarrollo clínico del cangrelor como terapia coadyuvante en la ICP se basó en el programa CHAMPION, del que se interrumpieron prematuramente los 2 primeros estudios (CHAMPION PCI5 y CHAMPION PLATFORM6) por futilidad, atribuible en parte a una definición restrictiva de infarto de miocardio3,7. En cambio, el ensayo CHAMPION PHOENIX sí demostró la superioridad del cangrelor frente al clopidogrel en la reducción de la variable principal de eficacia (combinado de muerte, infarto de miocardio, revascularización guiada por isquemia o trombosis de stent) a las 48 horas en pacientes en los que se realizaba ICP por angina estable o cualquier tipo de síndrome coronario agudo (SCA), y que no podían haber recibido pretratamiento con un iP2Y12 oral1. Cabe mencionar que, en un análisis conjunto de los 3 ensayos, el cangrelor mostró un ligero aumento del riesgo hemorrágico, fundamentalmente a expensas de sangrados menores8; este buen perfil de seguridad es probable que se deba a que el fármaco se administra durante un tiempo muy limitado y su efecto desaparece rápido tras parar la infusión.
Se han planteado 2 críticas importantes al diseño del ensayo CHAMPION PHOENIX que pueden condicionar su implementación en la práctica clínica en nuestro medio. La primera es que no se ha comparado el cangrelor con el prasugrel o el ticagrelor (más potentes y eficaces que el clopidogrel, y de elección en pacientes con SCA) y la segunda es haber considerado como criterio de exclusión el pretratamiento con iP2Y12 antes de la ICP. Cabe recordar que, pese a existir serias dudas sobre el beneficio del pretratamiento en el SCA, en especial en el SCA sin elevación persistente del segmento ST9, esta estrategia está ampliamente extendida en nuestro país. De hecho, en la ficha técnica europea del fármaco se especifica que el cangrelor está indicado, en asociación con ácido acetilsalicílico, en pacientes «que se someten a ICP, que no han recibido un inhibidor oral de P2Y12 antes del procedimiento de ICP y en quienes el tratamiento oral con inhibidores de P2Y12 no es posible o deseable»2. Pese a ello, las características farmacológicas del cangrelor hacen que sea particularmente interesante en situaciones en las que no solo el mencionado pretratamiento no se haya producido, sino también en circunstancias en las que este se considere insuficiente. Buena prueba de ello es la experiencia publicada del registro nacional sueco (SCAAR) durante los 2 primeros años de utilización del fármaco, en el que se halló un uso casi exclusivo del cangrelor en pacientes con IAMCEST en los que se realizaba angioplastia primaria; en este estudio de vida real, el cangrelor se combinó mayoritariamente con ticagrelor, aunque este se había administrado en más del 50% de las ocasiones en el ámbito prehospitalario, por lo que en dichos casos el uso del cangrelor sería considerado fuera de indicación (off-label)10.
Los escenarios clínicos en los que el cangrelor, en nuestra opinión, podría ser de utilidad, tanto en el contexto de la ICP (la gran mayoría de los casos) como en otras situaciones, se exponen en la figura 1. El escenario más relevante sería el de la angioplastia primaria en el IAMCEST, en la cual es apropiado su uso si no ha habido pretratamiento adecuado con iP2Y12 por imposibilidad o dificultad de administración de fármacos orales (intubación o vómito incoercible); también puede valorarse si se considera que la dosis de carga de los iP2Y12 no es efectiva durante el procedimiento (breve espacio de tiempo desde su administración hasta la ICP). Otra situación propicia (a priori mucho menos frecuente que la anterior) sería la ICP no emergente considerada de alto riesgo (p. ej., bifurcación con técnica de 2 stents, intervención multivaso, gran carga trombótica, etc.) en pacientes sin pretratamiento con iP2Y12. En cualquier caso, siempre habrá que ponderar el potencial beneficio del fármaco para prevenir eventos trombóticos intraprocedimiento con el riesgo hemorrágico del paciente y del procedimiento. Además, hay que recordar que no es pertinente utilizar cangrelor si se tiene la intención de administrar un inhibidor de la glucoproteína IIb/IIIa.
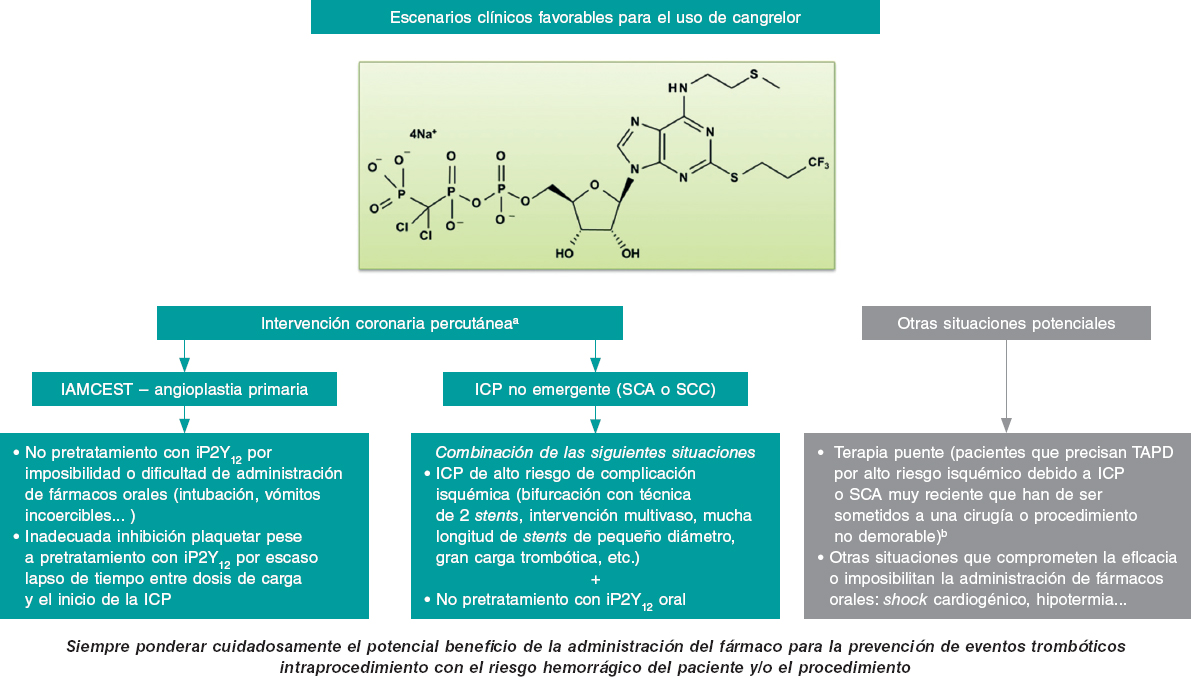
Figura 1. Escenarios clínicos potencialmente favorables para el uso del cangrelor. IAMCEST: infarto agudo de miocardio con elevación persistente del segmento ST; ICP: intervención coronaria percutánea; iP2Y12: inhibidores del receptor plaquetario P2Y12; SCA: síndrome coronario agudo; SCC: síndrome coronario crónico; TAPD: tratamiento antiplaquetario doble.
aLa dosis en el contexto del intervencionismo coronario percut?eo es de 30 μg/kg en bolo seguido de infusi? a raz? de 4 μg/kg/min.
bLa dosis estudiada en terapia puente es una infusi? de 0,75 μg/kg/min.
Otros aspectos que consideramos relevantes son la duración de la infusión, que puede ser razonable mantenerla al menos 2 horas tras acabar la ICP. Según la ficha técnica, se debe iniciar antes del procedimiento y continuar durante al menos 2 horas o el tiempo que dure el procedimiento, lo que sea más largo, aunque esto puede no ser suficiente en situaciones con demora del inicio de acción de los fármacos orales. También es importante tener precaución al hacer la transición a los fármacos orales; de manera general, la recomendación es que el ticagrelor se puede administrar en cualquier momento (antes, durante o después de parar la infusión) y las tienopiridinas al acabar la infusión (de modo que se evite una interacción que comportaría un lapso de tiempo sin la antiagregación apropiada)3.
Teniendo en cuenta todo lo anterior, el cangrelor debería usarse primordialmente en la sala de cardiología intervencionista en situaciones de alto riesgo trombótico periprocedimiento cuando el pretratamiento con un iP2Y12 oral no se ha producido o se considera no recomendable o insuficiente. La disponibilidad del fármaco no parece que a corto plazo vaya a suponer un cambio radical en nuestra estrategia antiagregante en la ICP, pero hay situaciones (en especial la angioplastia primaria) en las que su singular perfil farmacológico va a resultar muy útil. Por ello, es esperable que su uso vaya aumentando poco a poco en la comunidad de cardiólogos intervencionistas a medida que se familiaricen con el fármaco. En suma, podemos concluir que el cangrelor representa una adición muy interesante al arsenal terapéutico del que disponemos en la ICP, dado que puede contribuir a individualizar, y por tanto optimizar, la estrategia antitrombótica.
CONFLICTO DE INTERESES
J.L. Ferreiro declara haber recibido honorarios por ponencias de Eli Lilly Co., Daiichi Sankyo, Inc., AstraZeneca, Roche Diagnostics, Pfizer, Abbott, Boehringer Ingelheim, Bristol-Myers Squibb y Ferrer; honorarios por consultorías de AstraZeneca, Eli Lilly Co., Ferrer, Boston Scientific, Pfizer, Boehringer Ingelheim, Daiichi Sankyo, Inc., Bristol-Myers Squibb; y becas de investigación de AstraZeneca. J.A. Gómez-Hospital declara haber recibido honorarios por consultorías de Abbott, Medtronic, Boston Scientific, Terumo e IHT.
BIBLIOGRAFÍA
1. Bhatt DL, Stone GW, Mahaffey KW, et al. Effect of platelet inhibition with cangrelor during PCI on ischemic events. N Engl J Med. 2013;368:1303-1313.
2. Kengrexal. Ficha técnica o resumen de las características del producto. Disponible en:https://cima.aemps.es/cima/pdfs/es/ft/115994001/FT_115994001.pdf. Consultado 18 May 2020.
3. Marcano AL, Ferreiro JL. Role of New Antiplatelet Drugs on Cardiovascular Disease:Update on Cangrelor. Curr Atheroscler Rep. 2016;18:66.
4. Ferreiro JL, Sánchez-Salado JC, Gracida M, et al. Impact of mild hypothermia on platelet responsiveness to aspirin and clopidogrel:an in vitro pharmacodynamic investigation. J Cardiovasc Transl Res. 2014;7:39-46.
5. Harrington RA, Stone GW, McNulty S, et al. Platelet inhibition with cangrelor in patients undergoing PCI. N Engl J Med. 2009;361:2318-2329.
6. Bhatt DL, Lincoff AM, Gibson CM, et al. Intravenous platelet blockade with cangrelor during PCI. N Engl J Med. 2009;361:2330-2341.
7. White HD, Chew DP, Dauerman HL, et al. Reduced immediate ischemic events with cangrelor in PCI:a pooled analysis of the CHAMPION trials using the universal definition of myocardial infarction. Am Heart J. 2012;163:182-190.e4.
8. Steg PG, Bhatt DL, Hamm CW, et al. Effect of cangrelor on periprocedural outcomes in percutaneous coronary interventions:a pooled analysis of patient-level data. Lancet. 2013;382:1981-1992.
9. Ferreiro JL. Pre-Treatment With Oral P2Y12 Inhibitors in Non-ST-Segment Elevation Acute Coronary Syndromes:Does One Size Fit All?JACC Cardiovasc Interv. 2020;13:918-920.
10. Grimfjärd P, Lagerqvist B, Erlinge D, Varenhorst C, James S. Clinical use of cangrelor:nationwide experience from the Swedish Coronary Angiography and Angioplasty Registry (SCAAR). Eur Heart J Cardiovasc Pharmacother. 2019;5:151-157.
Autor para correspondencia: Servicio de Cardiología, Hospital Universitario de Bellvitge – IDIBELL, Feixa Llarga s/n, 08907 L’Hospitalet de Llobregat, Barcelona, España.
Correo electrónico: jlferreiro@bellvitgehospital.cat (J.L. Ferreiro).