RESUMEN
Introducción y objetivos: La reestenosis de stents coronarios (RS) presentan altas tasas de necesidad de revascularización, y el balón farmacoactivo (BFA) presenta clase I (nivel de evidencia A) en su tratamiento. La eficacia de esta estrategia a muy largo plazo en pacientes no seleccionados es desconocida. Se pretende evaluar la eficacia del BFA en un registro de pacientes de la práctica clínica a muy largo plazo de seguimiento (5 años).
Métodos: Registro retrospectivo de una cohorte formada por pacientes con RS tratados con BFA. El evento primario fue la tasa de revascularización de la lesión tratada (RLT) con BFA a 5 años. Se valoraron eventos secundarios según los criterios Academic Research Consortium-2.
Resultados: Entre enero de 2010 y diciembre de 2013 se usó BFA de forma eficaz en 53 RS de 48 pacientes. Los pacientes presentaban edad avanzada (69,3 ± 11,8 años) y alta prevalencia de diabetes (55,8%). La tasa de RLT a 1 año fue del 9,4%, y del 20,8% a los 3 y 5 años. La tasa de RLT tardía (más allá del año de seguimiento) fue del 11,4%, tan solo en reestenosis de stent convencional. La RLT a 5 años no se asoció a diabetes (22,7 frente a 19,2%; p = 0,76) ni fue significativamente menor con el uso de balón de corte (12,5 frente a 24,3%; p = 0,47) o en reestenosis de stent convencional (20,6 frente a 21,1%; p = 0,96). No hubo casos de trombosis de stent definitiva/probable de la lesión tratada con BFA.
Conclusiones: En una cohorte de la práctica clínica, el BFA para RS presenta una RLT a 5 años del 20,8%. La RLT tardía supone la mitad de los casos a lo largo del seguimiento, y se produce en RS convencional. La tasa de RLT parece estabilizarse a partir del tercer año de seguimiento. No se evidenció trombosis de stent de la lesión tratada con BFA.
Palabras clave: Balón farmacoactivo. Reestenosis de stent. Revascularización de lesión tratada.
ABSTRACT
Introduction and objectives: Coronary in-stent restenosis (ISR) is associated with a high target lesion revascularization rate, while the drug-eluting balloon (DEB) presents IA class level of evidence for its treatment. Nevertheless, very long-term outcomes of DEB for ISR in non-selected populations of patients are unknown. Our goal is to evaluate the very long-term (5 year) effectiveness of DEBs in a real-world registry.
Methods: Retrospective registry from an ISR cohort treated with DEB. The primary outcome was the rate of target lesion revascularization (TLR) at 5 years. Secondary outcomes were evaluated according to the ARC-2 criteria.
Results: From January 2010 through December 2013, 53 ISRs were treated using DEBs in 48 patients. Patients were old (69.3 ± 11.8 years-old) and 55.8% had diabetes. The rate of TLR at 1 year was 9.4%, and 20.8% at 3 and 5 years, respectively. The rate of late TLR (after the first year) was 11.4%, only after DEB for bare metal ISR. The 5-year TLR was not associated with diabetes (22.7% vs 19.2%; P = .76), and was not significantly lower after cutting-balloon (12.5% vs 24.3%; P = .47) or in bare-metal stent ISR (20.6% vs 21.1%; P = .96). There was no definite/probable stent thrombosis of the lesions treated with DEB at follow-up.
Conclusions: In a real-world cohort, the 5-year TLR rate after DEB for ISR was 20.8%. Late TLR accounted for half of the TLR at follow-up (after DEB for bare metal ISR), while the rate of TLR seemed to stabilize at 3 years. There was no stent thrombosis of the lesions treated with DEB.
Keywords: Drug-eluting balloon. In-stent restenosis. Target lesion revascularization.
Abreviaturas: BFA: balón farmacoactivo; RLT: revascularización de lesión tratada; RS: reestenosis de stent coronario; SFA: stent farmacoactivo; SM: stent metálico; TAPD: tratamiento antiagregante plaquetario doble.
INTRODUCCIÓN
La reestenosis de los stents coronarios (RS) sigue siendo un problema habitual y un reto terapéutico debido a las altas tasas de necesidad de revascularización de la lesión causante. El tratamiento de elección en la RS sigue sin estar establecido1. Según diversos estudios aleatorizados, la angioplastia con balón farmacoactivo (BFA) presenta en la RS mejores resultados que la angioplastia convencional y similares resultados que el implante in-stent de stents farmacoactivos (SFA) de primera generación2-13,aunque cierta desventaja frente a los SFA de segunda generación (máxime en RS de SFA)14,15. Esta estrategia tiene actualmente indicación de clase I (nivel de evidencia A) para el tratamiento de la RS tanto de stents metálicos (SM) como de SFA16.
La eficacia de esta estrategia a largo plazo (más de 1 año de seguimiento) se ha descrito en la literatura17-22, pero es testimonial a muy largo plazo (más allá de los 3 años)23. De igual manera, los estudios consideran como criterio de exclusión presentar una alta comorbilidad, por lo que el efecto es desconocido en pacientes del mundo real no seleccionados.
Se propone evaluar la eficacia del BFA en un registro de pacientes de la práctica clínica a muy largo plazo de seguimiento (5 años).
MÉTODOS
Registro retrospectivo de una cohorte formada por pacientes con RS tratados con BFA en un centro con alto volumen de procedimientos (> 1.500/año) y de intervenciones coronarias percutáneas (> 800/año). Se definió RS como la estenosis angiográfica superior al 50% en 2 proyecciones radiológicas ortogonales dentro del stent o a menos de 5 mm de sus bordes, junto con síntomas de angina o demostración objetiva de isquemia. Todas las lesiones se trataron con el mismo BFA (SeQuent Please, B. Braun Surgical, Melsungen, Alemania). No se establecieron criterios de exclusión clínicos ni angiográficos en el registro.
Las características clínicas y del procedimiento se obtuvieron de las bases de datos del centro y del laboratorio de cateterismo cardiaco. Se realizó un análisis coronario cuantitativo de las lesiones con el sistema Philips Xcelera. Se utilizó la clasificación de reestenosis de Mehran para la categorización de las lesiones24. La estrategia del procedimiento y la predilatación con balones de corte o balones no distensibles a alta presión fue a criterio del operador. La dilatación con el BFA se realizó durante al menos 60 segundos, como mínimo a presión nominal.
Se estableció un periodo de seguimiento de 5 años. El estudio fue autorizado por el Comité de Ensayos Clínicos. Todos los seguimientos se realizaron por criterios clínicos a través de consulta de la base de datos electrónica del sistema sanitario regional, en donde se detallan de forma exhaustiva todos los contactos del paciente con el mismo.
Todos los eventos se definieron de forma estandarizada según el consenso Academic Research Consortium-2 (ARC-2)25. El evento primario fue la necesidad de revascularización de la lesión tratada (RLT) con el BFA y se calculó sobre el cómputo total de lesiones tratadas. Los eventos secundarios fueron cualquier revascularización, síndrome coronario agudo/infarto agudo de miocardio según la definición universal de la Sociedad Europea de Cardiología (la misma o cualquier localización)26, muerte por cualquier causa y cardiovascular, hemorragia según el Bleeding Academic Research Consortium (BARC) ≥ 327 y los eventos combinados orientados al dispositivo (DOCE [device-oriented composite endpoints]: RLT + síndrome coronario agudo/infarto agudo de miocardio vaso causante + muerte cardiovascular) o al paciente (POCE [patient-oriented composite endpoints]: cualquier revascularización + síndrome coronario agudo/infarto agudo de miocardio + ictus + muerte total), y se calcularon sobre el cómputo total de pacientes. La trombosis de stent también se definió según criterios ARC-2, e igualmente se calculó sobre el cómputo total de lesiones.
La compilación y el análisis de los datos se realizaron con el programa IBM SPSS 19.0. Las variables cuantitativas se expresaron como media ± desviación estándar, y las variables cualitativas se expresaron como porcentaje relativo. Se estimó la incidencia acumulada de los eventos a lo largo del tiempo de seguimiento. Se realizó un análisis bivariado con test de χ2 o test exacto de Fisher, y una regresión logística multinomial para la estimación de predictores del evento primario (valor estadísticamente significativo: p < 0,05). Se utilizó el método de Kaplan-Meier para construir la curva de incidencia acumulada en el tiempo de seguimiento del evento primario.
RESULTADOS
Se trataron con BFA de forma eficaz 53 RS en 48 pacientes entre enero de 2010 y diciembre de 2013. En un paciente el BFA no consiguió cruzar la lesión, por lo que no se incluyó en el estudio (tasa de éxito del procedimiento con BFA del 98,2%). Las características basales, de las lesiones y del intervencionismo coronario se detallan en la tabla 1 y la tabla 2. El 49,1% (n = 26) de las lesiones presentaban un patrón de reestenosis Mehran I y un 24,5% (n = 13) presentaban afectación de bordes del stent. En todos los pacientes se obtuvo un buen resultado angiográfico (estenosis residual < 30%) y un flujo TIMI (Thrombolysis in Myocardial Infarction) de 3. La mediana de seguimiento fue 5,6 años (rango: 0,2-8,2 años). No hubo pérdidas en el seguimiento.
Tabla 1. Características basales de los pacientes
| Características de los pacientes | n = 48 |
|---|---|
| Edad (años) | 69,3 ± 11,8 (44-93) |
| Varón | 77,1% (37) |
| HTA | 75% (36) |
| Dislipemia | 56,3% (27) |
| Tabaquismo | 35,4% (17) |
| Diabetes | |
| DM + ADO | 33,3% (16) |
| DMID | 12,5% (6) |
| Fibrilación auricular (ACO) | 22,4% (11) |
| IM previo | 43,8% (21) |
| Indicación ICP previa | |
| CI estable | 37,5% (18) |
| SCA | 62,5% (30) |
| CABG previa | 6,3% (3) |
| IRC (FG < 60 ml/min) | 41,3% (19) |
| FEVI (%) | 55 ± 10,2 (65-29) |
| Enfermedad multivaso | 77,1% (37) |
| Revascularización incompleta | 18,9% (9) |
| Inhibidores P2Y12 | |
| Clopidogrel | 95,8% (46) |
| Ticagrelor/prasugrel | 4,2% (2) |
| Tiempo TAPD | |
| 3 meses | 22,4% (11) |
| 6 meses | 33,3% (16) |
| 12 meses | 43,8% (21) |
| IECA/ARA-II | 87,5% (42) |
| Bloqueadores beta | 91,7% (44) |
| Estatinas | 100% (48) |
ACO: anticoagulantes orales; ADO: antidiabéticos orales; ARA-II: antagonistas del receptor de la angiotensina II; CABG: cirugía de revascularización coronaria; CI: cardiopatía isquémica; DM: diabetes mellitus; DMID: diabetes mellitus dependiente de insulina; FG: filtrado glomerular; FEVI: fracción de eyección del ventrículo izquierdo; HTA: hipertensión arterial; ICP: intervención coronaria percutánea; IECA: inhibidores de la enzima de conversión de la angiotensina; IM: infarto de miocardio; IRC: insuficiencia renal crónica; SCA: síndrome coronario agudo; TAPD: tratamiento antiagregante plaquetario doble. | |
Tabla 2. Características de las lesiones y del procedimiento
| Características lesión/ICP | n = 53 |
|---|---|
| Localización | |
| Descendente anterior | 50,9% (27) |
| Circunfleja | 15,1% (8) |
| Coronaria derecha | 26,4% (14) |
| Tronco coronario izquierdo | 5,7% (3) |
| Injerto aortocoronario venoso | 1,9% (1) |
| Bifurcación | 26,4% (14) |
| RS difusa (Mehran II, III, IV) | 50,9% (27) |
| RS bordes stent | 24,5% (13) |
| Tipo stent RS | |
| SM | 64,2% (34) |
| SFA | 22,6% (12) |
| SFA sobre SM previo | 7,5% (4) |
| SFA sobre SFA previo | 5,7% (3) |
| SFA segunda generación/total SFA | 84,2% (16) |
| Stent ≥ 3 mm | 66% (35) |
| Diámetro stent (mm) | 2,9 ± 0,4 (2-4) |
| Longitud stent (mm) | 22,8 ± 7,1 (8-38) |
| Diámetro BFA (mm) | 3,1 ± 0,3 (2-3,5) |
| Longitud BFA (mm) | 20 ± 5,3 (15-30) |
| QCA antes de la ICP | |
| Diámetro referencia (mm) | 3,08 ± 0,39 |
| Diámetro luminal mínimo (mm) | 0,9 ± 0,43 |
| Estenosis (% diámetro) | 62 ± 15 |
| Longitud | 13 ± 5,3 |
| QCA tras la ICP | |
| Diámetro referencia (mm) | 3,1 ± 0,36 |
| Diámetro luminal mínimo (mm) | 2,27 ± 0,35 |
| Estenosis (% diámetro) | 15 ± 6 |
| Balón de corte | 30,2% (16) |
| Balón no distensible | 62,3% (33) |
| Acceso radial | 55,1% (27) |
| Éxito ICP (estenosis residual < 30%) | 100% (53) |
BFA: balón farmacoactivo; ICP: intervención coronaria percutánea; QCA: análisis coronario cuantitativo; RS: reestenosis de stent; SFA: stent farmacoactivo; SM:stent metálico. | |
La mayoría de los pacientes (95,8%, n = 46) recibieron clopidogrel como inhibidor del receptor P2Y12 para el tratamiento antiagregante plaquetario doble (TAPD), y el 22,4% (n = 11) se encontraban en tratamiento con anticoagulantes orales y recibieron pautas cortas de TAPD (3 meses).
La tasa de RLT a 1 año fue del 9,4%, y a los 3 y 5 años fue del 20,8%. La tasa de RLT tardía (más allá del año de seguimiento) fue del 11,4%. En el análisis de Kaplan-Meier (figura 1) puede apreciarse que los eventos se acumularon durante los primeros 3 años. La tasa de RLT a 1 año fue significativamente menor en RS de SM (2,9 frente a 21,1%; p = 0,05), y no se observó TLR tardía en RS de SFA. La tasa de RLT a 5 años no se asoció a diabetes (22,7 frente a 19,2%; p = 0,76) y no fue significativamente menor con el uso de balón de corte (12,5 frente a 24,3%; p = 0,47), en stents ≥ 3 mm (25,7 frente a 11,1%; p = 0,29) ni en RS de SM (20,6 frente a 21,1%; p = 0,96). En el análisis bivariado y en la regresión logística no se identificaron variables que actuaran como predictores independientes de RLT.
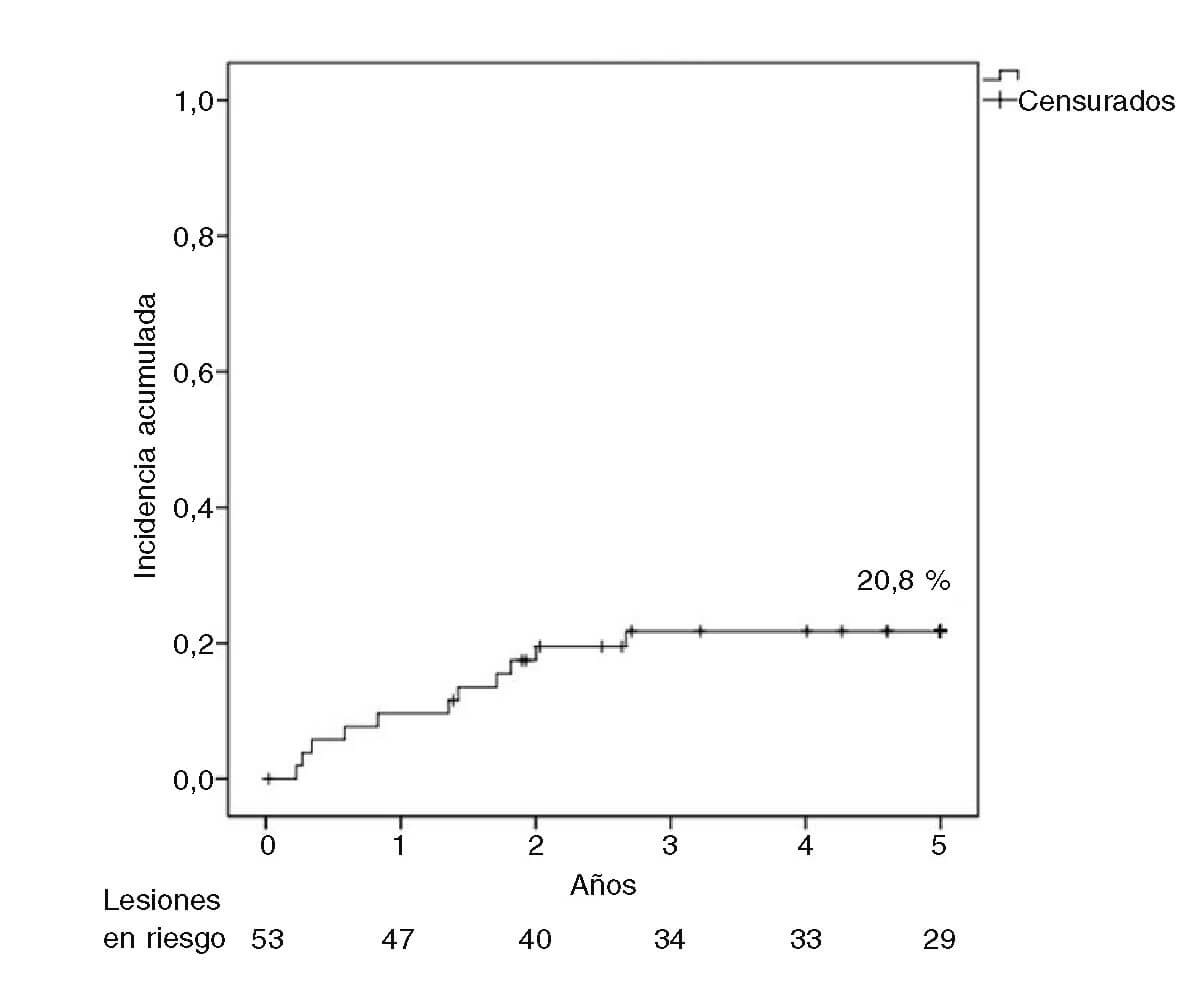
Figura 1. Análisis de Kaplan-Meier sobre la incidencia acumulada de revascularización de la lesión tratada (RLT) a lo largo de 5 años de seguimiento.
No hubo casos de trombosis de stent en la lesión tratada. Se produjeron 2 síndromes coronarios agudos/infarto agudo de miocardio dependientes del vaso tratado: 1 debido a otra lesión proximal a la lesión tratada con BFA (esta presentaba buen resultado) y tan solo un caso de síndrome coronario agudo/infarto agudo de miocardio sin elevación de ST por nueva RS de la lesión tratada con BFA.
Durante el seguimiento se realizó nueva coronariografía al 50% de los pacientes (n = 24). En el 29,2% (n = 14) de los pacientes se dispuso de verificación angiográfica de ausencia de nueva RS en el stent tratado con BFA. Un paciente presentó 2 RLT en 2 lesiones distintas durante el seguimiento.
Los restantes eventos secundarios y compuestos se detallan en la tabla 3. La mortalidad global a 5 años fue del 33,3% (n = 16), y las neoplasias fueron la causa más frecuente (n = 5). Según los criterios ARC-2, la mortalidad por causa cardiovascular fue del 10,4% (n = 5): 2 muertes súbitas pasados 3 años de seguimiento (ambos con coronariografía previa y buen resultado de las lesiones tratadas con BFA) y 3 ictus pasados 2 años de seguimiento (uno hemorrágico bajo anticoagulación oral).
Tabla 3. Eventos secundarios y compuestos a 5 años de seguimiento
| Eventos secundarios a 5 años | n = 48 |
|---|---|
| Cualquier revascularización | 29,2% (14) |
| SCA-IM vaso tratado | 4,2% (2) |
| SCA-IM otra localización | 10,4% (5) |
| Mortalidad total | 33,3% (16) |
| Mortalidad de causa cardiovascular | 10,4% (5) |
| Ictus | 12,5% (6) |
| DOCE | 31,3% (15) |
| POCE | 54,2% (26) |
| Hemorragia BARC ≥ 3 | 6,3% (3) |
BARC: Bleeding Academic Research Consortium; DOCE: device-oriented composite endpoints; IM: infarto agudo de miocardio; POCE: patient-oriented composite endpoints; SCA:síndrome coronario agudo. | |
El 27,1% (n = 13) de los pacientes presentaron hemorragia durante el seguimiento, aunque solo el 6,3% (n = 3) estaban en trata- miento con TAPD (1 de ellos con anticoagulación oral). Tres pacientes presentaron hemorragia BARC ≥ 3: un paciente con hemorragia gastrointestinal BARC 3a y 2 pacientes con hemorragia BARC 5b (1 por hemorragia gastrointestinal en TAPD y otro por hemorragia intracraneal bajo anticoagulación oral).
DISCUSIÓN
Desde nuestro conocimiento, el estudio que se presenta es el primero que describe a muy largo plazo la evolución de las lesiones de RS tratadas con BFA en pacientes no seleccionados (fuera de un ensayo clínico) pertenecientes al mundo real (edad avanzada y alto riesgo cardiovascular). De nuestra serie pueden extraerse las siguientes conclusiones: a) aunque la tasa de RLT al año es similar a la de los estudios publicados, a largo plazo parece ser mayor que la descrita en pacientes seleccionados; b) la RLT tardía (más allá del año de seguimiento) supone la mitad de los casos de necesidad de nueva revascularización a lo largo del seguimiento; c) a largo plazo, la RLT es similar en RS en SM y SFA, pero la RLT tardía solo aparece en RS de SM; d) la tasa de RLT parece estabilizarse a partir de los 3 años; y e) el uso de BFA en el tratamiento de RS es una estrategia segura desde el punto de vista de la trombosis del stent, incluso en pacientes que reciben estrategias cortas de TAPD.
Los resultados a medio plazo (6-12 meses) del uso de BFA en el tratamiento de RS han sido ampliamente descritos en estudios aleatorizados en los que se comparaba esta estrategia frente a angioplastia simple o implante de SFA, en poblaciones con criterios de exclusión clínicos y angiográficos. Scheller et al.3 comunicaron inicialmente en el estudio PACCOCATH - ISR (Treatment of in-Stent Restenosis by Paclitaxel Coated PTCA Balloons) una RLT angiográfica a 6 meses del 0% y una RLT clínica a 12 meses del 4%. Posteriores investigaciones comunican datos más ajustados a los resultados reales, con RLT a medio plazo del 6,6-8,8%2,7,8,10,13-15, con diferencias en función de si era RS en SM (6-8,7%)2,5,14 o en SFA (4,3-22,1%)4,6-8,13,15,28. Alfonso et al.14,15 han comunicado en los estudios RIBS (Restenosis Intra-stent of Bare Metal Stents: Paclitaxel-eluting Balloon vs Everolimus-eluting Stent) V y IV (poblaciones con similar situación geográfica a la nuestra) una RLT al año del 6 y del 13% en RS de SM y SFA, respectivamente. En estos 2 trabajos se comunicaron 26 RLT en 249 pacientes (95 con SM y 154 con SFA), lo que conllevaría una tasa del 10,4%, muy similar al 9,4% de nuestra serie.
Diversos estudios han publicado el seguimiento a 3 años: PEPCAD21 y RIBS V19 en SM, y RIBS IV20, PEPCAD-DES22 e ISAR-DESIRE 318 en SFA, con RLT del 6,2, 8, 15,6, 19,4 y 33,3%, respectivamente. En estos trabajos se han comunicado en total 94 RLT en 524 lesiones, lo que supondría una RLT a 3 años del 17,9%, inferior al 20,8% de nuestra serie. Aunque en nuestra muestra la diabetes no se asoció a RLT, es un potente predictor de RS29. Este hallazgo podría justificarse por una prevalencia mucho mayor de diabetes en nuestra muestra (55,5%) que en la de los estudios descritos (32-40%).
Se define como RLT tardía aquella que aparece por encima del año de seguimiento. En los estudios publicados se enfatiza que la RLT se concentra durante el primer año de seguimiento y luego es poco relevante, con tasas entre el 0 y el 4,1% (0-25% casos del total). En nuestra serie, la RLT tardía fue del 11,4%, lo que supuso más de la mitad de los casos (54% de todas las RLT). Tan solo en el estudio ISAR-DESIRE18 y el trabajo de Habara et al.30 se describen tasas de RLT tardía más cercanas a las de nuestro estudio (14,5 y 7,2%, respectivamente; 43 y 39% de todas las RLT). Las diferencias entre los estudios aleatorizados y nuestra serie, en la que la RLT es clínica, podrían explicarse porque la mayoría de los pacientes tienen seguimiento angiográfico durante el primer año, lo que podría haber puesto de manifiesto precozmente en pacientes asintomáticos una nueva RS angiográficamente significativa (> 50%), pero sin magnitud suficiente para producir clínica.
En nuestra serie tan solo hubo casos de RLT tardía en SM, ya que todas las RLT en SFA ocurrieron dentro del primer año de seguimiento. Inicialmente, la efectividad del BFA fue mayor en RS de SM, pero la incidencia de RLT aumentó en el seguimiento y se igualó a la del grupo de SFA (figura 2). Estos resultados podrían explicarse por el mayor efecto inicial del BFA sobre el patrón característico en RS de SM (células musculares lisas) frente al patrón de neoaterosclerosis, más común en RS de SFA28, y esta misma neoaterosclerosis es la causante de los eventos tardíos en los SM, tal como describieron Nakazawa et al.31. Nuestros resultados difieren de los publicados por Habara et al.30 en una larga serie (550 lesiones en 468 pacientes), en la que la RLT tardía aparece preferentemente en RS de SFA (odds ratio = 6; p = 0,002). Si bien los autores comunican que no hubo diferencias en las tasas de RLT entre SFA de primera y segunda generación, el 70% de los SFA fueron de primera generación (14% stents de paclitaxel), frente al 15% en nuestra serie (3 stents de sirolimus y ninguno de paclitaxel). El seguimiento de este estudio finaliza a los 2 años, por lo que resta aclarar si a más largo plazo persistirían estos hallazgos.
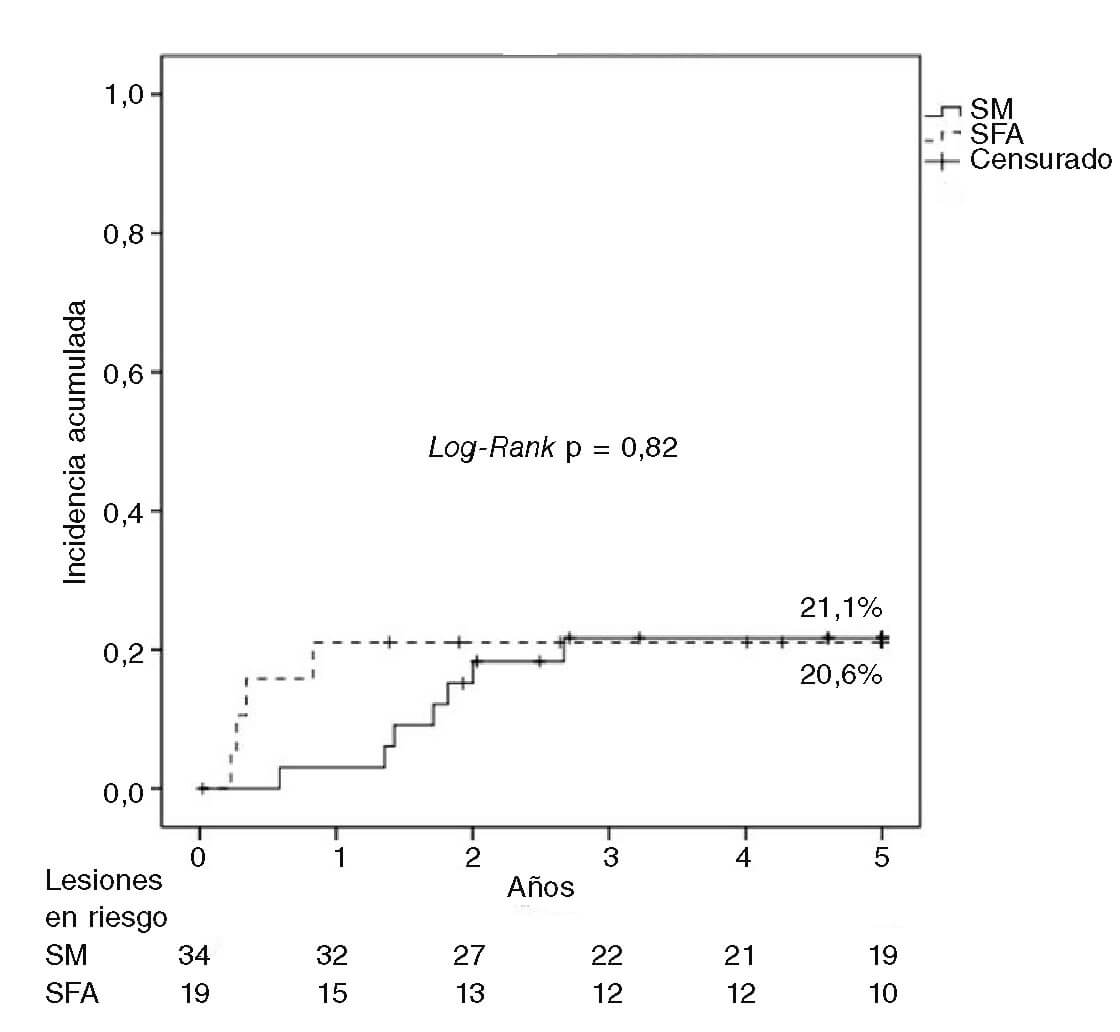
Figura 2. Análisis de Kaplan-Meier sobre la revascularización de la lesión tratada (RLT) a 5 años tras el uso de balón farmacoacti- vo en reestenosis de stent metálico (SM) frente a stent farmaco- activo (SFA).
Scheller et al.23 publicaron el seguimiento a 5 años del PACCOCATH- ISR, con RLT a 5 años del 9,3% y una prevalencia de diabetes del 17%. Miura et al.32 comunicaron una RLT del 34% a 5 años en 216 RS de SFA, tasa mucho mayor que la evidenciada en nuestra muestra, con una prevalencia similar de diabetes. Ambos trabajos sugieren que la RLT sigue aumentando a largo plazo. Curiosamente, en nuestra serie la RLT se estabiliza a partir del tercer año. En estos trabajos se describen casos de RLT entre los 2 y 5 años, pero no se especifica en qué momento aparecen. Es posible que la RLT clínica tras BFA pueda ocurrir más allá del año de seguimiento (1-3 años), y que posteriormente se estabilice en el tiempo.
En el estudio ISAR-DESIRE 4, el uso de balón de corte en el tratamiento de la RS con BFA ha obtenido mejores resultados angiográficos (reestenosis binaria) y una reducción no significativa de la RLT al año (16,2 frente a 21,8%; p = 0,26)33. En nuestra serie, los pacientes tratados con balón de corte presentaron una tasa de RLT numéricamente inferior (12,5 frente a 24,3%), pero sin significación estadística debido al tamaño muestral. Solo el 30% de las lesiones se trataron con esta técnica, ya que en el momento del estudio no estaba establecido su beneficio33.
Nuestra muestra presentaba 2 características con escasa información en la literatura: edad avanzada y uso de anticoagulación oral. La edad media era de casi 70 años, con datos de pacientes extremadamente añosos (hasta 93 años) y más del 20% tomaban anticoagulantes orales. Si bien esto no supone un criterio de exclusión, los estudios publicados no detallan el porcentaje de pacientes en tratamiento con anticoagulación oral, y no comunican la tasa de hemorragias en el seguimiento18-22. En dichos estudios, la TAPD se prolongó entre 3 y 6 meses. En nuestra serie, más del 50% de los pacientes fueron tratados con una estrategia de 3-6 meses con TAPD, y aquellos que recibían anticoagulación oral (22,4%) siguieron una estrategia de 3 meses. El uso de BFA con estas pautas fue seguro. La tasa total de hemorragias fue moderada, como corresponde a la edad, y solo un paciente presentó hemorragia BARC ≥ 3 bajo TAPD. Pese al alto porcentaje de pacientes con pautas cortas de TAPD, no hubo casos de trombosis definitiva/probable de la lesión tratada. Salvo en el estudio PEPCAD, en el que tampoco se comunicó trombosis del stent de la lesión tratada con BFA, el resto de los trabajos comunicaron tasas a largo plazo entre el 0,8% (ISAR-DESIRE) y el 2,6% (RIBS IV)18-22.
Los criterios ARC-2 son criterios de consenso para homogeneizar resultados, aunque en población de edad avanzada y alto riesgo isquémico pueden penalizar la eficacia de la intervención. La elevada tasa de DOCE a 3 años (31,3%) se magnificó por la mortalidad de causa cardiovascular (10,4%), que según los criterios ARC-2 debe incluir también la atribuible a ictus. Como se ha descrito, por cronología y causa es difícil que la mortalidad cardiovascular de nuestra muestra pueda atribuirse al BFA. Pese a ser eventos combinados con diferentes definiciones, los DOCE podrían asemejarse a los clásicos MACE (major adverse cardiac events), con una incidencia similar a la descrita en los trabajos publicados, en torno al 20-38% a 3 años18-22. El alto riesgo isquémico de nuestros pacientes se evidencia por las altas tasas de síndrome coronario agudo/infarto agudo de miocardio no dependiente de la lesión tratada (10,2%) e ictus (12,5%) durante el seguimiento. Ambos eventos, junto con la alta mortalidad de causa no cardiovascular asociada a la edad (neoplasias), penalizaron los POCE, que doblando a los DOCE en nuestra muestra (54,2%). Así pues, aproximadamente la mitad de los eventos combinados según los criterios ARC-2 en el seguimiento a 5 años no serían atribuibles al uso de BFA.
Limitaciones
Nuestro trabajo presenta varias limitaciones. Se trata de un estudio retrospectivo, unicéntrico y con una casuística limitada que no permite obtener una fuerte evidencia. En línea con los resultados previos descritos en la literatura, los nuestros apoyan el uso de BFA para el tratamiento de la RS, de manera que, a largo plazo, aproximadamente en el 80% de los pacientes de una población no seleccionada podría evitarse tener que implantar una capa adicional de SM y podría reservarse esta estrategia para el fracaso del BFA.
CONCLUSIONES
En una cohorte de la práctica clínica, el BFA para RS presenta una RLT a 5 años del 20,8%. La RLT tardía supone la mitad de los casos a lo largo del seguimiento, y aparece en RS de SM. La tasa de RLT parece estabilizarse a partir del tercer año de seguimiento. No se evidenció trombosis de stent de la lesión tratada con BFA.
CONFLICTO DE INTERESES
Ninguno.
¿QUÉ SE SABE DEL TEMA?
- El uso de BFA para el tratamiento de la RS es una estrategia validada por estudios aleatorizados con seguimientos entre 1 y 3 años en poblaciones seleccionadas, con tasas de RLT en torno al 8-10% al año. La efectividad de esta estrategia a 5 años está descrita en la literatura de forma testimonial.
- La RLT tardía (tras 1 año de seguimiento) tiene poca relevancia en los citados estudios.
¿QUÉ APORTA DE NUEVO?
- La efectividad y el seguimiento a muy largo plazo (5 años) del uso de BFA para RS en una población no seleccionada de alto riesgo cardiovascular. Aunque la RLT al año es similar a la observada en los estudios aleatorizados, en una cohorte del mundo real la RLT tardía podría ser más importante que la descrita en los estudios (sobre todo en stents convencionales), y aunque parece estabilizarse a partir del tercer año, es más elevada en el seguimiento a muy largo plazo (5 años).
- En los pacientes con alto riesgo de hemorragia, las pautas cortas de TAPD no se asociaron a trombosis de stent de la lesión tratada con BFA.
BIBLIOGRAFÍA
1. Alfonso F, Byrne RA, Rivero F, Kastrati A. Current treatment of in-stent restenosis. J Am Coll Cardiol. 2014;63:2659-2673.
2. Pleva L, Kukla P, Kusnierova P, Zapletalova J, Hlinomaz O. CompaRSon of the Efficacy of Paclitaxel-Eluting Balloon Catheters and Everolimus-Eluting Stents in the Treatment of Coronary In-Stent Restenosis:The Treatment of In-Stent Restenosis Study. Circ Cardiovasc Interv. 2016;9:e003316.
3. Scheller B, Hehrlein C, Bocksch W, et al. Treatment of coronary in-stent restenosis with a paclitaxel-coated balloon catheter. N Engl J Med. 2006;355:2113-2124.
4. Habara S, Iwabuchi M, Inoue N, et al. A multicenter randomized comparison of paclitaxel-coated balloon catheter with conventional balloon angioplasty in patients with bare-metal stent restenosis and drug-eluting stent restenosis. Am Heart J. 2013;166:527-533.
5. Unverdorben M, Vallbracht C, Cremers B, et al. Paclitaxel-coated balloon catheter versus paclitaxel-coated stent for the treatment of coronary in-stent restenosis. Circulation. 2009;119:2986-2994.
6. Rittger H, Brachmann J, Sinha AM, et al. A randomized, multicenter, single-blinded trial comparing paclitaxel-coated balloon angioplasty with plain balloon angioplasty in drug-eluting stent restenosis:the PEPCAD-DES study. J Am Coll Cardiol. 2012;59:1377-1382.
7. Habara S, Mitsudo K, Kadota K, et al. Effectiveness of paclitaxel-eluting balloon catheter in patients with sirolimus-eluting stent restenosis. JACC Cardiovasc Interv. 2011;4:149-154.
8. Byrne RA, Neumann FJ, Mehilli J, et al. Paclitaxel-eluting balloons, paclitaxel-eluting stents, and balloon angioplasty in patients with restenosis after implantation of a drug-eluting stent (ISAR-DESIRE 3):a randomised, open- label trial. Lancet. 2013;381:461-467.
9. Indermuehle A, Bahl R, Lansky AJ, et al. Drug-eluting balloon angioplasty for in-stent restenosis:a systematic review and meta-analysis of randomised controlled trials. Heart. 2013;99:327-333.
10. Baan J, Jr., Claessen BE, Dijk KB, et al. A Randomized Comparison of Paclitaxel-Eluting Balloon Versus Everolimus-Eluting Stent for the Treatment of Any In-Stent Restenosis:The DARE Trial. JACC Cardiovasc Interv. 2018;11:275-283.
11. Siontis GC, Stefanini GG, Mavridis D, et al. Percutaneous coronary interventional strategies for treatment of in-stent restenosis:a network meta-analysis. Lancet. 2015;386:655-664.
12. Giacoppo D, Gargiulo G, Aruta P, Capranzano P, Tamburino C, Capodanno D. Treatment strategies for coronary in-stent restenosis:systematic review and hierarchical Bayesian network meta-analysis of 24 randomised trials and 4880 patients. BMJ. 2015;351:h5392.
13. Xu B, Gao R, Wang J, et al. A prospective, multicenter, randomized trial of paclitaxel-coated balloon versus paclitaxel-eluting stent for the treatment of drug-eluting stent in-stent restenosis:results from the PEPCAD China ISR trial. JACC Cardiovasc Interv. 2014;7:204-211.
14. Alfonso F, Perez-Vizcayno MJ, Cardenas A, et al. A randomized comparison of drug-eluting balloon versus everolimus-eluting stent in patients with bare-metal stent-in-stent restenosis:the RIBS V Clinical Trial (Restenosis Intra-stent of Bare Metal Stents:paclitaxel-eluting balloon vs. everolimus-eluting stent). J Am Coll Cardiol. 2014;63:1378-1386.
15. Alfonso F, Perez-Vizcayno MJ, Cardenas A, et al. A Prospective Randomized Trial of Drug-Eluting Balloons Versus Everolimus-Eluting Stents in Patients With In-Stent Restenosis of Drug-Eluting Stents:The RIBS IV Randomized Clinical Trial. J Am Coll Cardiol. 2015;66:23-33.
16. Neumann FJ, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2018;40:87-165.
17. Xu B, Qian J, Ge J, et al. Two-year results and subgroup analyses of the PEPCAD China in-stent restenosis trial:A prospective, multicenter, randomized trial for the treatment of drug-eluting stent in-stent restenosis. Catheter Cardiovasc Interv. 2016;87(Suppl 1):624-629.
18. Kufner S, Cassese S, Valeskini M, et al. Long-Term Efficacy and Safety of Paclitaxel-Eluting Balloon for the Treatment of Drug-Eluting Stent Restenosis:3-Year Results of a Randomized Controlled Trial. JACC Cardiovasc Interv. 2015;8:877-884.
19. Alfonso F, Perez-Vizcayno MJ, Garcia Del Blanco B, et al. Long-Term Results of Everolimus-Eluting Stents Versus Drug-Eluting Balloons in Patients With Bare-Metal In-Stent Restenosis:3-Year Follow-Up of the RIBS V Clinical Trial. JACC Cardiovasc Interv. 2016;9:1246-1255.
20. Alfonso F, Perez-Vizcayno MJ, Cuesta J, et al. 3-Year Clinical Follow-Up of the RIBS IV Clinical Trial:A Prospective Randomized Study of Drug-Eluting Balloons Versus Everolimus-Eluting Stents in Patients With In-Stent Restenosis in Coronary Arteries Previously Treated With Drug-Eluting Stents. JACC Cardiovasc Interv. 2018;11:981-991.
21. Unverdorben M, Vallbracht C, Cremers B, et al. Paclitaxel-coated balloon catheter versus paclitaxel-coated stent for the treatment of coronary in-stent restenosis:the three-year results of the PEPCAD II ISR study. EuroIntervention. 2015;11:926-934.
22. Rittger H, Waliszewski M, Brachmann J, et al. Long-Term Outcomes After Treatment With a Paclitaxel-Coated Balloon Versus Balloon Angioplasty:Insights From the PEPCAD-DES Study (Treatment of Drug-eluting Stent [DES] In-Stent Restenosis With SeQuent Please Paclitaxel-Coated Percutaneous Transluminal Coronary Angioplasty [PTCA] Catheter). JACC Cardiovasc Interv. 2015;8:1695-1700.
23. Scheller B, Clever YP, Kelsch B, et al. Long-term follow-up after treatment of coronary in-stent restenosis with a paclitaxel-coated balloon catheter. JACC Cardiovasc Interv. 2012;5:323-330.
24. Mehran R, Dangas G, Abizaid AS, et al. Angiographic patterns of in-stent restenosis:classification and implications for long-term outcome. Circulation.1999;100:1872-1878.
25. Garcia-Garcia HM, McFadden EP, Farb A, et al. Standardized End Point Definitions for Coronary Intervention Trials:The Academic Research Consortium-2 Consensus Document. Circulation. 2018;137:2635-2650.
26. Thygesen K, Alpert JS, Jaffe AS, et al. Fourth universal definition of myocardial infarction (2018). Eur Heart J. 2019;40:237-269.
27. Mehran R, Rao SV, Bhatt DL, et al. Standardized bleeding definitions for cardiovascular clinical trials:a consensus report from the Bleeding Academic Research Consortium. Circulation. 2011;123:2736-2747.
28. Alfonso F, Perez-Vizcayno MJ, Garcia Del Blanco B, et al. Usefulness of Drug-Eluting Balloons for Bare-Metal and Drug-Eluting In-Stent Restenosis (from the RIBS IV and V Randomized Trials). Am J Cardiol. 2017;119:983-990.
29. Cassese S, Byrne RA, Tada T, et al. Incidence and predictors of restenosis after coronary stenting in 10 004 patients with surveillance angiography. Heart. 2014;100:153-159.
30. Habara S, Kadota K, Shimada T, et al. Late Restenosis After Paclitaxel-Coated Balloon Angioplasty Occurs in Patients With Drug-Eluting Stent Restenosis. J Am Coll Cardiol. 2015;66:14-22.
31. Nakazawa G, Otsuka F, Nakano M, et al. The pathology of neoatherosclerosis in human coronary implants bare-metal and drug-eluting stents. J Am Coll Cardiol. 2011;57:1314-1322.
32. Miura K, Kadota K, Habara S, et al. Five-Year Outcomes After Paclitaxel-Coated Balloon Angioplasty for Drug-Eluting Stent Restenosis. Am J Cardiol. 2017;119:365-371.
33. Kufner S, Joner M, Schneider S, et al. Neointimal Modification With Scoring Balloon and Efficacy of Drug-Coated Balloon Therapy in Patients With Restenosis in Drug-Eluting Coronary Stents:A Randomized Controlled Trial. JACC Cardiovasc Interv. 2017;10:1332-1340.
Corresponding author: Sección de Cardiología Intervencionista, Servicio de Cardiología, Hospital Clínico Universitario Lozano Blesa, Avda. San Juan Bosco 15, 05009 Zaragoza, España.
Correo electrónico: joselinares1979@hotmail.com (J.A. Linares Vicente).